题目内容
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法是还原沉淀法。该法的工艺流程为: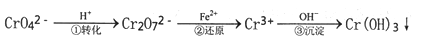
其中第①步存在平衡:2 CrO42-(黄色)+2H+ Cr2O72- (橙色)+H2O
Cr2O72- (橙色)+H2O
(1) 若平衡体系的pH=12,则溶液显_______色。
(2) 能说明第①步反应达平衡状态的是______________。
a.Cr2O72-和CrO42-的浓度不变
B.2v(Cr2O72-) =v(CrO42-)
C.溶液的颜色不变
(3)第②步中,还原lmol Cr2O72-离子,需要_______mol的FeSO4•7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr (OH)3 (s) Cr3+ (aq) +3OH- (aq)
Cr3+ (aq) +3OH- (aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-) = 10-32,要使0.01mol/Lc(Cr3+)开始沉淀,溶液的pH应调至__________,若使c(Cr3+)降至10-5mol/L,溶液的pH应调至___________。
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g) 2NH3(g) ΔH=-92.6 kJ·mol-1。
2NH3(g) ΔH=-92.6 kJ·mol-1。
实验测得起始、平衡时的有关数据如下表所示:
容器 编号 | 起始时各物质的物质的量/mo | 达平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15 kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述错误的是
A.容器①、②中反应的平衡常数相等
B.容器②中达平衡时放出的热量Q=23.15 kJ
C.若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
D.平衡时,两个容器中NH3的体积分数相等


 也是正四面体
也是正四面体