题目内容
CH3+、-CH3(甲基)、CH3-都是重要的有机反应中间体,有关它们的说法正确的是 ( )
| A、它们均由甲烷去掉一个氢原子所得 | B、它们互为等电子体,碳原子均采取sp2杂化 | C、CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形 | D、CH3+中的碳原子采取sp2杂化,所有原子均共面 |
分析:A.甲烷去掉一个氢原子不能得到CH3+、CH3-;
B.CH3+、-CH3、CH3-分别具有6个、7个和8个价电子,不是等电子体;
C.CH3-与NH3、H3O+均具有10个电子,互为等电子体;
D.CH3+中的碳原子采取sp2杂化.
B.CH3+、-CH3、CH3-分别具有6个、7个和8个价电子,不是等电子体;
C.CH3-与NH3、H3O+均具有10个电子,互为等电子体;
D.CH3+中的碳原子采取sp2杂化.
解答:解:A.甲烷分子变成CH3+、-CH3、CH3-时,失去的分别是氢负离子、氢原子和氢离子,空间构型也不再与原来的分子相同,故A错误;
B.CH3+、CH3-、CH3-分别具有6个、7个和8个价电子,不是等电子体,中心碳原子的价层电子对数不同,故空间构型不同,故B错误;
C.CH3-与NH3、H3O+均具有8个价电子,4个原子,互为等电子体,几何构型均为三角锥形,故C正确;
D.CH3+中的碳原子采取sp2杂化,平面三角形结构,所有原子均共面,故D正确;
故选CD.
B.CH3+、CH3-、CH3-分别具有6个、7个和8个价电子,不是等电子体,中心碳原子的价层电子对数不同,故空间构型不同,故B错误;
C.CH3-与NH3、H3O+均具有8个价电子,4个原子,互为等电子体,几何构型均为三角锥形,故C正确;
D.CH3+中的碳原子采取sp2杂化,平面三角形结构,所有原子均共面,故D正确;
故选CD.
点评:本题考查离子构型的判断、杂化方式的判断等知识点,题目难度中等,根据价层电子对互斥理论来分析解答即可,注意明确CH3+、-CH3(甲基)、CH3-的区别.

练习册系列答案
相关题目
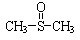 ),有关反应如下:
),有关反应如下: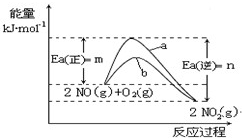
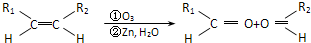
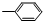 ③-CH═CH2
③-CH═CH2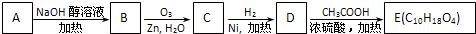
 +NaOH
+NaOH +NaCl+H2O
+NaCl+H2O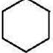
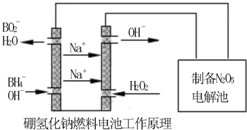 二甲基亚砜
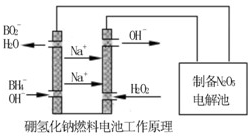
二甲基亚砜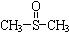 有消炎止痛、镇静等作用.甲醇和硫化氢在γ-Al2O3催化剂作用下生成甲硫醚(CH3-S-CH3),甲硫醚再与NO2反应制取二甲基亚砜(
有消炎止痛、镇静等作用.甲醇和硫化氢在γ-Al2O3催化剂作用下生成甲硫醚(CH3-S-CH3),甲硫醚再与NO2反应制取二甲基亚砜(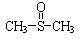 ),有关反应如下:
),有关反应如下: