题目内容
【题目】电池式氧传感器原理构造如图,可测定O2的含量。工作时铅极表面会逐渐附着Pb(OH)2。下列说法不正确的是
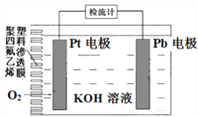
A. Pt电极上发生还原反应
B. 随着使用,电解液的pH逐渐减小
C. a ×10-3molO2反应,理论上可使Pb电极增重68a mg
D. Pb电极上的反应式为Pb+2OH--2e-=Pb(OH)2
【答案】B
【解析】A.Pt电极上O2得电子生成OH-,发生还原反应,故A正确;B.铅失电子在负极发生氧化反应生成Pb(OH)2,电极反应式为Pb+2OH--2e-=Pb(OH)2,O2在正极Pt上得电子生成OH-,电极反应式为O2+2H2O+4e-=4OH-,总反应为:2Pb+O2+2H2O=2Pb(OH)2,消耗水,电解液碱性增强,所以电解液的pH逐渐增大,故B错误;C.a×10-3molO2反应则得到4a×10-3mol电子,所以根据得失电子守恒,理论上可使Pb电极增重4a×10-3mol×17g/mol=68a×10-3g=68amg,故C正确;D.铅失电子在负极发生氧化反应生成Pb(OH)2,电极反应式为Pb+2OH--2e-=Pb(OH)2,故D正确;故选B。

【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向苯酚浊液中滴加Na2CO3溶液,浊液变清 | 苯酚的酸性强于H2CO3的酸性 |
B | 将溴乙烷和氢氧化钠的乙醇溶液共热后产生的气体通入溴的四氯化碳溶液,溶液褪色 | 溴乙烷发生消去反应 |
C |
|
|
D | 向 |
|
A.AB.BC.CD.D
【题目】在稀氨水中存在下述电离平衡NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”“减小”或“不变”);平衡移动方向如何?(填“正向”“逆向”或“不移动”)
NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”“减小”或“不变”);平衡移动方向如何?(填“正向”“逆向”或“不移动”)
加入的物质 | 少量(NH4)2SO4固体 | 少量HNO3溶液 | 少量KOH溶液 |
c(OH-)的变化 | |||
平衡移动方向 |