题目内容
实验室用浓盐酸、MnO2共热制取Cl2,并用Cl2和Ca(OH)2反应制取少量漂白粉,现已知反应2Cl2+2Ca(OH)2====Ca(ClO)2+CaCl2+2H2O,温度稍高即发生副反应:6Cl2+6Ca(OH)2====Ca(ClO3)2+5CaCl2+6H2O。现有三个同学分别设计三套实验装置如下:
(1)请从:a.不容易控制反应速率,b.容易控制反应速率,c.有副反应发生,d.可防止副反应发生,e.污染环境,f.可防止污染环境几个方面对上述甲、乙、丙三套装置的优缺点作出评价,并选择符合题目要求的选项填在空格内。
装置 | 优点 | 缺点 |
甲 |
|
|
乙 |
|
|
丙 |
|
|
(2)图中甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G组成,从下述甲、乙、丙三套装置中选出合理的部分(按气流从左到右的方向)组装一套较完善的实验装置(填所选部分的编号):_____________________。
(3)实验中若用12 mol·L-1的浓盐酸100 mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总小于0.15 mol,其可能的主要原因是____________________________(假定各步反应均无反应物损耗且无副反应发生)。
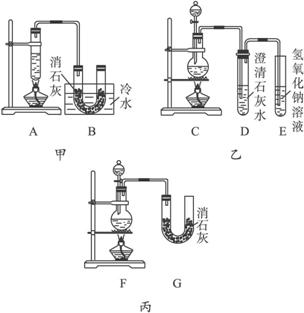
图6-31
解析:本题综合性较强,既要熟悉Cl2的制法,又要抓住题给信息应用理论知识,采取相应的实验措施。根据题给药品,制取Cl2应选用装置C或F。依据题给信息Cl2与Ca(OH)2的反应是放热反应,且温度高时易发生副反应,所以制漂白粉时应采取降温措施。Cl2有毒,又需进行尾气处理。
答案:(1)①优点d;缺点a、e ②优点f;缺点a、c ③优点b;缺点c、e
(2)F→B→E
(3)浓盐酸逐渐变稀,稀盐酸与MnO2不反应,且浓盐酸易挥发,所以盐酸不能全部反应生成Cl2,故生成的Ca(ClO)2小于0.15 mol

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案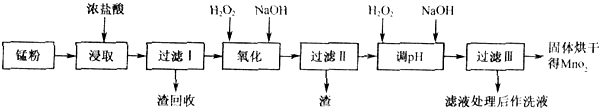
根据如图所示步骤并参考表格数据,回答下列问题.
生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
(2)锰粉经浓盐酸浸取,过滤I除去不溶杂质后,向滤液中加入足量H2O2溶液,其作用是
(3)过滤Ⅰ所得滤液经氧化后,需加入NaOH溶液调节pH约为5.1,其目的是
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离子方程式为
(5)实验室进行过滤操作时.需要用到的玻璃仪器有
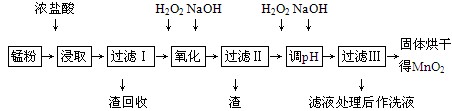
回收的废旧锌锰干电池经过处理后得到锰粉(含MnO2、Mn(OH)2、Fe、乙炔和黑炭等),由锰粉制取MnO2的步骤如下图所示。
生成氢氧化物沉淀的pH
|
物质 |
开始沉淀 |
沉淀完全 |
|
Fe(OH)3 |
2.7 |
3.7 |
|
Fe(OH)2 |
7.6 |
9.6 |
|
Mn(OH)2 |
8.3 |
9.8 |
根据上图所示步骤并参考表格数据,回答下列问题。
(1)在加热条件下用浓盐酸浸取锰粉,所得溶液中含有Mn2+、Fe2+等。MnO2与浓盐酸反应的离子方程式为___________________________________________
(2)锰粉经浓盐酸浸取,过滤Ⅰ除去不溶杂质后,向滤液中加入足量H2O2溶液,其作用是____________________________________________________________。
(3)过滤Ⅰ所得滤液经氧化后,需加入NaOH溶液调节pH约为5.1,其目的是___________________________________________________________。
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离子方程式为_____________________________________________。
(5)实验室进行过滤操作时,需要用到的玻璃仪器有________________________