题目内容
“绿色化学”是21世纪化学发展的主导方向,“绿色化学”的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染,并使原子利用率为100%.下列符合“绿色化学”的是( )
①用甲烷、一氧化碳合成乙酸乙酯:2CH4+2CO
CH3COOC2H5
②氢氧燃料电池
③在通风橱进行有毒气体的实验
④对工业生产硝酸产生的废气废水进行严格处理
⑤生产环氧乙烷:CH2=CH2+Cl2+Ca(OH)2→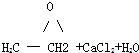
⑥2M+N=2P+2Q,2P+M=Q (M、N为原料,Q为期望产品)
①用甲烷、一氧化碳合成乙酸乙酯:2CH4+2CO
| 催化剂 |
②氢氧燃料电池
③在通风橱进行有毒气体的实验
④对工业生产硝酸产生的废气废水进行严格处理
⑤生产环氧乙烷:CH2=CH2+Cl2+Ca(OH)2→
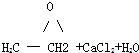
⑥2M+N=2P+2Q,2P+M=Q (M、N为原料,Q为期望产品)
| A、①③④⑥ | B、①②⑤ |
| C、①②③④ | D、①②⑥ |
分析:原子利用率为100%即要使原料中的原子全部转入到产品中,做到零排放,从生成物来看,生成物必须是一种,反应类型应是化合反应或加成反应.
解答:解:①用甲烷、一氧化碳合成乙酸乙酯:2CH4+2CO
CH3COOC2H5,该反应是化合反应,原子利用率为100%,故①正确;
②氢氧燃料电池,电池反应式2H2+O2=2H2O,该反应是化合反应,原子利用率为100%,故②正确;
③在通风橱进行有毒气体的实验,不符合绿色化学的含义,故③错误;
④对工业生产硝酸产生的废气废水进行严格处理,可通过下列反应处理:NO+NO2+2NaOH=2NaNO2+H2O,该反应不是化合反应,原子利用率不为100%,故④错误;
⑤生产环氧乙烷:CH2=CH2+Cl2+Ca(OH)2→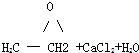 ,该反应不是化合反应,原子利用率不为100%,故⑤错误;
,该反应不是化合反应,原子利用率不为100%,故⑤错误;
⑥2M+N=2P+2Q,2P+M=Q,总反应:3M+N=3Q,该反应是化合反应,原子利用率为100%,故⑥正确;
故选:D.
| 催化剂 |
②氢氧燃料电池,电池反应式2H2+O2=2H2O,该反应是化合反应,原子利用率为100%,故②正确;
③在通风橱进行有毒气体的实验,不符合绿色化学的含义,故③错误;
④对工业生产硝酸产生的废气废水进行严格处理,可通过下列反应处理:NO+NO2+2NaOH=2NaNO2+H2O,该反应不是化合反应,原子利用率不为100%,故④错误;
⑤生产环氧乙烷:CH2=CH2+Cl2+Ca(OH)2→
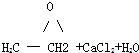 ,该反应不是化合反应,原子利用率不为100%,故⑤错误;
,该反应不是化合反应,原子利用率不为100%,故⑤错误;⑥2M+N=2P+2Q,2P+M=Q,总反应:3M+N=3Q,该反应是化合反应,原子利用率为100%,故⑥正确;
故选:D.
点评:解答本题要抓住一个主要信息:“化学反应绿色化”要求原料物质中所含原子完全被利用并且全部转入期望的产品中,反应类型应是化合反应或加成反应.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目