题目内容
在指定环境中,下列各组离子可以大量共存的是( )
分析:A.利用离子的相互促进水解来分析;
B.由水电离的c(OH-)=10-14mol?L-1的溶液,为酸或碱溶液;
C.在pH=11的溶液,为碱溶液;
D.根据氧化还原反应及复分解反应来分析.
B.由水电离的c(OH-)=10-14mol?L-1的溶液,为酸或碱溶液;
C.在pH=11的溶液,为碱溶液;
D.根据氧化还原反应及复分解反应来分析.
解答:解:A.因Al3+、HCO3-发生相互促进水解的反应,则不能共存,故A错误;
B.由水电离的c(OH-)=10-14mol?L-1的溶液,为酸或碱溶液,酸溶液中Fe2+、NO3-发生氧化还原反应,Fe2+、ClO-发生氧化还原反应,碱溶液中氢氧根离子分别与Fe2+、NH4+结合,则不能共存,故B错误;
C.在pH=11的溶液,为碱溶液,该组离子之间不反应,则能够共存,故C正确;
D.酸性溶液中,I-、NO3-发生氧化还原反应,氢离子与AlO2-结合生成沉淀,则不能共存,故D错误;
故选C.
B.由水电离的c(OH-)=10-14mol?L-1的溶液,为酸或碱溶液,酸溶液中Fe2+、NO3-发生氧化还原反应,Fe2+、ClO-发生氧化还原反应,碱溶液中氢氧根离子分别与Fe2+、NH4+结合,则不能共存,故B错误;
C.在pH=11的溶液,为碱溶液,该组离子之间不反应,则能够共存,故C正确;
D.酸性溶液中,I-、NO3-发生氧化还原反应,氢离子与AlO2-结合生成沉淀,则不能共存,故D错误;
故选C.
点评:本题考查离子的共存,明确信息及离子之间的反应即可解答,题目难度不大,注意离子之间的氧化还原反应、相互促进水解等来解答.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
A 、B 、C 、D 、E 、F、G为原子序数依次增大的元素,其中前六种属于短周期元素。已知B 、C 、F 三种原子的最外层共有11 个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应并且生成盐和水。请完成下列问题:
(1)只根据以上条件一定能判断出的元素的及符合条件的离子的符号填写在下表空格处
| 编号 | A | B | C | D | E | F | G | 半径最小的离子 |
| 符号 |
 (2)写出B、C 的最高价氧化物对应的水化物间反
(2)写出B、C 的最高价氧化物对应的水化物间反
应的离子方程式____________
(3)己知D的单质在F单质中燃烧可生成X、Y两
种化合物并产生白色烟雾,写出X、Y中各原子
最外层均满足8 电子结构的分子的电子式___。
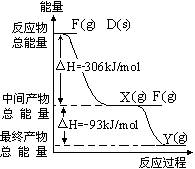
D、F的单质反应过程和能量关系如图所示(图
中的△H表示生成1mol产物的数据),写出指定
条件下两种单质作用生成Y时的热化学方程式
_______________________。
(4) G的单质是目前用途最广泛的一种金属材料,但在使用中受环境影响易被腐蚀,试写出发生腐蚀时的电极反应式_________________________________________。
(5)A与E能形成两种常见的化合物,这两种化合物中属于非极性分子的物质化学式_______