题目内容
工业上用丁烷氧化法制醋酸,反应的化学方程式可表示为:2C4H10+5O2
4CH3COOH+2H2O,现用58吨丁烷为原料制取醋酸,求:
(1)理论上需要标准状况下的空气
(2)若生成的醋酸溶解在生成的水中,所得醋酸的质量分数为
(3)若同时生产质量分数为100%的冰醋酸m1吨和质量分数为50%的醋酸m2吨,且
=x,需补充水y吨,则y与x的关系式为
| 一定条件 |
(1)理论上需要标准状况下的空气
2.8×105
2.8×105
m3(设空气中O2、N2的体积分数分别为0.2、0.8),同时生成水18
18
吨.(2)若生成的醋酸溶解在生成的水中,所得醋酸的质量分数为
86.96
86.96
%.(3)若同时生产质量分数为100%的冰醋酸m1吨和质量分数为50%的醋酸m2吨,且
| m1 |
| m2 |
y=
| 102-36x |
| 2x+1 |
y=
;若不补充水,则m1+m2=| 102-36x |
| 2x+1 |
138
138
.分析:(1)令O2需要的物质的量为xmol,根据方程式中计算氧气的物质的量,结合氧气在空气中的含量计算需要空气的体积;
令生成水y吨,根据方程式计算生成水的质量.
(2)令生成醋酸m吨,根据方程式计算生成醋酸的质量,根据质量分数的定义计算.(3)由题意可知,m1+50%×m2=120.若需补充水y吨,则50%×m2=18+y,所以m2=36+2y;所以m1=120-18-y=102-y.
若不补充水,50%×m2=18,所以m2=36,故m1=120-50%×m2=102.
令生成水y吨,根据方程式计算生成水的质量.
(2)令生成醋酸m吨,根据方程式计算生成醋酸的质量,根据质量分数的定义计算.(3)由题意可知,m1+50%×m2=120.若需补充水y吨,则50%×m2=18+y,所以m2=36+2y;所以m1=120-18-y=102-y.
若不补充水,50%×m2=18,所以m2=36,故m1=120-50%×m2=102.
解答:解:(1)令O2需要的物质的量为xmol,则:
2 C4H10+5O2
4CH3COOH+2H2O,
58×2g 5mol
58×106 xmol
所以x=
=2.5×106
所以需要空气的体积为
=2.8×108L=2.8×105m3.
令生成水y吨,则:
2 C4H10+5 O2
4CH3COOH+2H2O,
58×2g 18×2g
58吨 y吨
所以y=
=18
故答案为:2.8×105;18.
(2)令生成醋酸m吨,则:
2 C4H10+5 O2
4CH3COOH+2H2O,
58×2g 4×60g
58吨 m吨
所以m=
=120
由(1)中计算可知,生成水18吨,
生成的醋酸溶解在生成的水中,所得醋酸的质量分数为
×100%=86.96%.
故答案为:86.96%.
(3)由题意可知,m1+50%×m2=120,
若需补充水y吨,则50%×m2=18+y,所以m2=36+2y;所以m1=120-18-y=102-y,即102-y=x(36+2y),即y=
;
若不补充水,50%×m2=18,所以m2=36,故m1=120-50%×m2=102,所以m1+m2=36+102=138.
故答案为:y=
;138.
2 C4H10+5O2
| 一定条件 |
58×2g 5mol
58×106 xmol
所以x=
| 5×58×106 |
| 2×58 |
所以需要空气的体积为
| 2.5×106mol×22.4L/mol |
| 0.2 |
令生成水y吨,则:
2 C4H10+5 O2
| 一定条件 |
58×2g 18×2g
58吨 y吨
所以y=
| 58×2×18 |
| 58×2 |
故答案为:2.8×105;18.
(2)令生成醋酸m吨,则:
2 C4H10+5 O2
| 一定条件 |
58×2g 4×60g
58吨 m吨
所以m=
| 58×4×60 |
| 58×2 |
由(1)中计算可知,生成水18吨,
生成的醋酸溶解在生成的水中,所得醋酸的质量分数为
| 120吨 |
| 120吨+18吨 |
故答案为:86.96%.
(3)由题意可知,m1+50%×m2=120,
若需补充水y吨,则50%×m2=18+y,所以m2=36+2y;所以m1=120-18-y=102-y,即102-y=x(36+2y),即y=
| 102-36x |
| 2x+1 |
若不补充水,50%×m2=18,所以m2=36,故m1=120-50%×m2=102,所以m1+m2=36+102=138.
故答案为:y=
| 102-36x |
| 2x+1 |
点评:考查根据方程式的计算,难度中等,计算量较大,需细心计算,旨在考查学生对数据处理及利用方程式进行计算.

练习册系列答案
相关题目
 4CH3COOH+2H2O
4CH3COOH+2H2O 4CH3COOH+2H2O
4CH3COOH+2H2O ,需补充水y吨,则y与x的关系式为 (用含x的代数式表示y);若不补充水,则m1+m2= 。
,需补充水y吨,则y与x的关系式为 (用含x的代数式表示y);若不补充水,则m1+m2= 。 4CH3COOH+2H2O
4CH3COOH+2H2O ,需补充水y吨,则y与x的关系式为 (用含x的代数式表示y);若不补充水,则m1+m2= 。
,需补充水y吨,则y与x的关系式为 (用含x的代数式表示y);若不补充水,则m1+m2= 。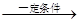 4CH3COOH+2H2O
4CH3COOH+2H2O ,需补充水y吨,则y与x的关系式为
(用含x的代数式表示y);若不补充水,则m1+m2=
。
,需补充水y吨,则y与x的关系式为
(用含x的代数式表示y);若不补充水,则m1+m2=
。