题目内容
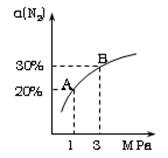
对于反应N2(g)+3H2(g)?2NH3(g);△H<0,下列研究目的和示意图相符的是( )
分析:由方程式可知,反应物气体的计量数大于生成物气体的计量数,则增大压强平衡向正反应方向移动,正反应放热,则升高温度平衡向逆反应方向移动,加入催化剂,正逆反应速率增大,但平衡不移动.
解答:解:A.反应物气体的计量数大于生成物气体的计量数,则增大压强平衡向正反应方向移动,氨气的体积分数增大,压强越大反应速率越大,图象不符,故A错误;
B.正反应放热,则升高温度平衡向逆反应方向移动,氮气的转化率降低,图象不符,故B错误;
C.增加氮气,正反应速率增大,加入氮气瞬间逆反应速率不变,然后逐渐增大,重新达到平衡状态,图象符合,故C正确;
D.加入催化剂,反应速率增大,达到平衡所用时间少,图象不符合,故D错误.
故选C.
B.正反应放热,则升高温度平衡向逆反应方向移动,氮气的转化率降低,图象不符,故B错误;
C.增加氮气,正反应速率增大,加入氮气瞬间逆反应速率不变,然后逐渐增大,重新达到平衡状态,图象符合,故C正确;
D.加入催化剂,反应速率增大,达到平衡所用时间少,图象不符合,故D错误.
故选C.
点评:本题考查化学平衡图象问题,题目难度不大,解答本题的关键是能正确分析反应特点,结合外界条件对平衡移动的影响分析,答题时注意图象曲线的变化趋势.

练习册系列答案
相关题目
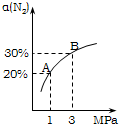 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )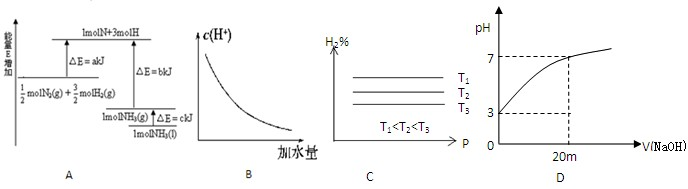
 2NH3(g) △H=-92.4kJ/mol。
2NH3(g) △H=-92.4kJ/mol。