题目内容
(10分)短周期元素X、Y、Z在周期表中位置关系如图:(答题时,X、Y、Z用所对应的元素符号表示)
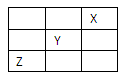
(1)x元素的单质分子式是_______,单质是_______晶体。
(2)自然界中存在一种仅含钙与Y两种元素的天然矿物,其电子式为_______,属于_______晶体。
(3)Z的氢化物和Y的氢化物沸点高低顺序是: ,理由:
。
(4)X、Y、Z三种元素中,电负性最大的是: 。

(1)x元素的单质分子式是_______,单质是_______晶体。
(2)自然界中存在一种仅含钙与Y两种元素的天然矿物,其电子式为_______,属于_______晶体。
(3)Z的氢化物和Y的氢化物沸点高低顺序是: ,理由:
。
(4)X、Y、Z三种元素中,电负性最大的是: 。
(1)He (1分) 分子(1分)
(2) (2分) 离子(1分)
(2分) 离子(1分)
(3)HF﹥H2S (2分) HF分子之间除了存在分子间作用力,还存在氢键。(2分)
(4) F (1分)
(2)
 (2分) 离子(1分)
(2分) 离子(1分)(3)HF﹥H2S (2分) HF分子之间除了存在分子间作用力,还存在氢键。(2分)
(4) F (1分)
根据短周期元素在周期表中的相对位置可知,元素X、Y、Z分别是He、F、S。
(1)稀有气体分子形成的晶体都是分子晶体。
(2)钙是第ⅡA元素,属于活泼的金属,最高价是+2价,所以和氟形成的化合物的化学式为CaF2,是离子键形成的离子晶体,其电子式为 。
。
(3)HF中含有氢键,所以其沸点高于硫化氢的。
(4)非金属性越强,大小越大,氟是最强的非金属,所以氟的电负性最大。
(1)稀有气体分子形成的晶体都是分子晶体。
(2)钙是第ⅡA元素,属于活泼的金属,最高价是+2价,所以和氟形成的化合物的化学式为CaF2,是离子键形成的离子晶体,其电子式为
 。
。(3)HF中含有氢键,所以其沸点高于硫化氢的。
(4)非金属性越强,大小越大,氟是最强的非金属,所以氟的电负性最大。

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
 CH ④NH3 ⑤NH4+⑥BF3 ⑦P4
CH ④NH3 ⑤NH4+⑥BF3 ⑦P4 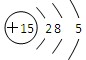 ,则该元素的位置为( )
,则该元素的位置为( )