题目内容
将Na2CO3、NaHCO3的混合物1.9g,强热至无气体出现为止,恢复至原来状态,称量剩余物的质量减轻了0.31g,求原混合物中NaHCO3质量分数.
【答案】分析:有关反应的方程式为:2NaHCO3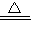 Na2CO3+CO2↑+H2O,利用差量法计算.
Na2CO3+CO2↑+H2O,利用差量法计算.
解答:解:设NaHCO3有xmol,
2NaHCO3 Na2CO3+CO2↑+H2O△m
Na2CO3+CO2↑+H2O△m
2mol 62g
xmol 0.31g
x= =0.01
=0.01
m(NaHCO3)=0.01mol×84g/mol=0.84g,
w(NaHCO3)=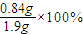 =44.2%.
=44.2%.
答:原混合物中NaHCO3质量分数为44.2%.
点评:本题考查混合物的额计算,题目难度不大,注意根据碳酸氢钠的性质,利用差量法计算.
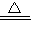 Na2CO3+CO2↑+H2O,利用差量法计算.
Na2CO3+CO2↑+H2O,利用差量法计算.解答:解:设NaHCO3有xmol,
2NaHCO3
 Na2CO3+CO2↑+H2O△m
Na2CO3+CO2↑+H2O△m2mol 62g
xmol 0.31g
x=
 =0.01
=0.01m(NaHCO3)=0.01mol×84g/mol=0.84g,
w(NaHCO3)=
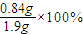 =44.2%.
=44.2%.答:原混合物中NaHCO3质量分数为44.2%.
点评:本题考查混合物的额计算,题目难度不大,注意根据碳酸氢钠的性质,利用差量法计算.

练习册系列答案
相关题目
(2012?上海模拟)从下列事实所得出的相应结论正确的是( )
|
将Na2CO3?10H2O和 NaHCO3的混合物n g,溶于水制成200mL溶液,测得c(Na+)=0.5mol/L.若将n g该混合物加热至质量不再改变时,得到的固体物质的质量为( )
| A、3.l g | B、5.3 g | C、9.0 g | D、11.0 g |