题目内容
【题目】化学社两位同学为探究铜跟浓硫酸的反应,设计了图所示装置. 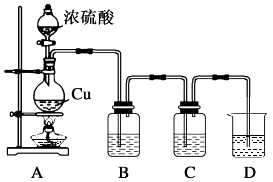
(1)反应开始前必须进行的操作是 .
(2)装置A中发生的反应的化学方程式为 .
(3)洗气瓶B中为品红溶液,确认有SO2生成的现象是 .
(4)洗气瓶C中为新制的氯水,反应的现象是新制氯水由淡黄绿色变为 , 原因是SO2具有性.
(5)烧杯D中盛装的试剂是浓度较大的溶液,其作用是
(6)若反应中有2mol电子转移,则生成的SO2在标准状况下的体积是 .
【答案】
(1)检验装置的气密性
(2)Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(3)品红溶液褪色
(4)无色;还原
(5)NaOH;防止SO2泄漏污染空气
(6)22.4 L
【解析】解:(1)反应是制取气体的装置,所以反应开始前必须要检验装置的气密性,所以答案是:检验装置的气密性;(2)Cu与浓硫酸反应生成硫酸铜、二氧化硫和水,反应的化学方程式为Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O,
CuSO4+SO2↑+2H2O,
所以答案是:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O;(3)二氧化硫能使品红溶液褪色,所以确认有SO2生成的现象是品红溶液褪色,所以答案是:品红溶液褪色;(4)二氧化硫与氯水中的氯气反应生成盐酸与硫酸,所以溶液由淡黄绿色变为无色;二氧化硫中硫的化合价升高是还原剂,具有还原性,所以答案是:无色;还原;(5)烧杯D是尾气处理的装置,盛装的试剂是浓度较大的可溶性的强碱溶液,可用氢氧化钠溶液,其作用是吸收二氧化硫气体,所以答案是:NaOH;防止SO2泄漏污染空气;(6)由反应Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;(3)二氧化硫能使品红溶液褪色,所以确认有SO2生成的现象是品红溶液褪色,所以答案是:品红溶液褪色;(4)二氧化硫与氯水中的氯气反应生成盐酸与硫酸,所以溶液由淡黄绿色变为无色;二氧化硫中硫的化合价升高是还原剂,具有还原性,所以答案是:无色;还原;(5)烧杯D是尾气处理的装置,盛装的试剂是浓度较大的可溶性的强碱溶液,可用氢氧化钠溶液,其作用是吸收二氧化硫气体,所以答案是:NaOH;防止SO2泄漏污染空气;(6)由反应Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O,若反应中有2mol电子转移,则生成1mol的SO2,标准状况下的体积为22.4L,所以答案是:22.4 L.
CuSO4+SO2↑+2H2O,若反应中有2mol电子转移,则生成1mol的SO2,标准状况下的体积为22.4L,所以答案是:22.4 L.