题目内容
【题目】按如图装置进行实验,并回答下列问题。
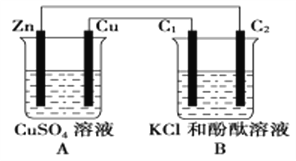
(1)判断装置的名称:A池为________,B池为________。
(2)锌极为________极,电极反应式为___________________________________。
铜极为________极,电极反应式为___________________________________。
石墨棒C1为________极,电极反应式为_________________________________。
石墨棒C2附近发生的实验现象为_______________________________________。
【答案】 原电池 电解池 负 Zn-2e-===Zn2+ 正 Cu2++2e-===Cu 阳 2Cl--2e-===Cl2↑ 有无色气体产生,附近溶液出现红色
【解析】该装置中A能自发的进行氧化还原反应为原电池,B为电解池,锌易失电子作负极,铜作正极,B中连接铜的电极为阳极,连接锌的电极为负极,电解池中阳极上氯离子放电,阴极上氢离子放电;A中锌电极上失电子生成锌离子进入溶液,铜电极上铜离子得电子生成铜单质,所以其电池反应式为Zn+Cu2+=Cu+Zn2+;(1)A能自发的进行氧化还原反应,能将化学能转化为电能,所以为原电池,B有外接电源,属于电解池;(2)该装置中A能自发的进行氧化还原反应为原电池,B为电解池,锌易失电子作负极,电极反应为:Zn-2e-=Zn2+;铜作正极,溶液中铜离子得到电子生成铜,电极反应为:Cu2++2e-=Cu;B中连接铜的电极为阳极,连接锌的电极为负极,电解池中阳极上氯离子放电,电极反应为:2Cl--2e-=Cl2↑;阴极上氢离子放电,电极反应为2H++2e-=H2↑,电极上有气体生成,溶液中水的电离平衡正向进行,氢氧根离子浓度增大,负极附近的溶液遇到酚酞变红色。

【题目】等电子体的结构相似、物理性质相近,称为等电子原理。如N2和CO为等电子体。下表为部分元素等电子体分类、空间构型表。
等电子体类型 | 代表物质 | 空间构型 |
四原子24电子等电子体 | SO3 | 平面三角形 |
四原子26电子等电子体 | SO32- | 三角锥形 |
五原子32电子等电子体 | CCl4 | 四面体形 |
六原子40电子等电子体 | PCl5 | 三角双锥形 |
七原子48电子等电子体 | SF6 | 八面体形 |
由第一、二周期元素组成,与F2互为等电子体的离子有__________。


