题目内容
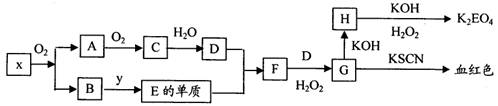
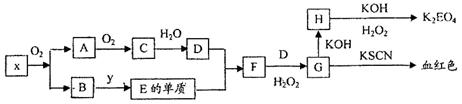
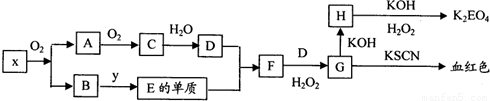
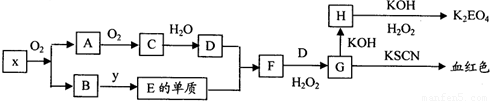
K2EO4(E代表某种元素)在工业上有重要的应用,以下是制备该物质的工艺流程图:
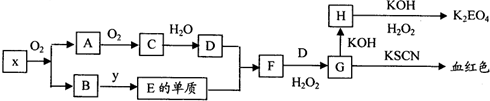
已知:A和C是由同一主族元素组成的化合物,x是工业上制D的重要原料.
请回答以下问题:
(1)x的化学式是
(2)写出F→G的离子反应方程式
(3)要实现B→E的转化,y的化学式可能是
(4)1molH转化为K2EO4时需H2O2的物质的量是

已知:A和C是由同一主族元素组成的化合物,x是工业上制D的重要原料.
请回答以下问题:
(1)x的化学式是
FeS2
FeS2
,H的化学式是Fe(OH)3
Fe(OH)3
.(2)写出F→G的离子反应方程式
2Fe2++2H++H2O2=2Fe3++2H2O
2Fe2++2H++H2O2=2Fe3++2H2O
.(3)要实现B→E的转化,y的化学式可能是
CO
CO
.(4)1molH转化为K2EO4时需H2O2的物质的量是
1.5mol
1.5mol
.分析:依据转化关系分析判断G为含Fe3+离子的溶液,H为Fe(OH)3,K2EO4应为K2FeO4,转化关系中F+H2O2=G,推断F含有Fe2+,E单质为Fe,D为酸,A和C是由同一主族元素组成的化合物,x是工业上制D的重要原料,结合A和氧气反应生成C,C溶于水生成D,推断A为SO2,C为SO3,D为H2SO4,说明x中含硫元素,结合B和Y反应生成Fe,推断x中含有铁元素,综合分析可知,x为FeS2,B为Fe2O3,Y为C、CO或H2;依据推断出的物质分析回答问题;
解答:解:依据转化关系分析判断G为含Fe3+离子的溶液,H为Fe(OH)3,K2EO4应为K2FeO4,转化关系中F+H2O2=G,推断F含有Fe2+,E单质为Fe,D为酸,A和C是由同一主族元素组成的化合物,x是工业上制D的重要原料,结合A和氧气反应生成C,C溶于水生成D,推断A为SO2,C为SO3,D为H2SO4,说明x中含硫元素,结合B和Y反应生成Fe,推断x中含有铁元素,综合分析可知,x为FeS2,B为Fe2O3,Y为C、CO或H2;F为FeSO4;G为Fe2(SO4)3;
(1)x的化学式为:FeS2;H的化学式为:Fe(OH)3;故答案为:FeS2; Fe(OH)3;
(2)F→G的反应是硫酸亚铁在酸性体积下被过氧化氢氧化为硫酸铁,本身被还原为水,反应的离子反应方程式为:
2Fe2++2H++H2O2=2Fe3++2H2O;
故答案为:2Fe2++2H++H2O2=2Fe3++2H2O;
(3)实现B→E的转化即Fe2O3→Fe,需要的是还原剂,可以是C、CO、H2、Al等;故答案为:CO;
(4)H转化为K2EO4时,发生的反应是2Fe(0H)3+4KOH+3H2O2=2K2FeO4+8H2O;1molH为Fe(OH)3转化为K2EO4时需H2O2的物质的量依据化学方程式计算得到物质的量是1.5mol;
故答案为:1.5mol;
(1)x的化学式为:FeS2;H的化学式为:Fe(OH)3;故答案为:FeS2; Fe(OH)3;
(2)F→G的反应是硫酸亚铁在酸性体积下被过氧化氢氧化为硫酸铁,本身被还原为水,反应的离子反应方程式为:
2Fe2++2H++H2O2=2Fe3++2H2O;
故答案为:2Fe2++2H++H2O2=2Fe3++2H2O;
(3)实现B→E的转化即Fe2O3→Fe,需要的是还原剂,可以是C、CO、H2、Al等;故答案为:CO;
(4)H转化为K2EO4时,发生的反应是2Fe(0H)3+4KOH+3H2O2=2K2FeO4+8H2O;1molH为Fe(OH)3转化为K2EO4时需H2O2的物质的量依据化学方程式计算得到物质的量是1.5mol;
故答案为:1.5mol;
点评:本题考查了物质转化的分析判断,物质性质的应用,反应过程的分析应用,特征反应的判断是解题关键,题目难度中等.

练习册系列答案
相关题目