题目内容
下列试验中,所选装置不合理的是

A. 粗盐提纯,选①和②
B. 用CC14提取碘水中的碘,选③
C. 用NaOH溶液吸收少量C12选⑤
D. 分离Na2CO3溶液和CH3COOC2H5,选④
练习册系列答案
相关题目
下列有关实验操作、发生的现象、解释或结论都正确的是( )
选项 | 实验操作 | 产生的现象 | 解释或结论 |
A | 向Na2SO3溶液中逐滴加入硝酸酸化的硝酸钡溶液 | 产生白色沉淀 | 产生的BaSO3是难溶于水的沉淀 |
B | 将SO2通入滴有酸性高锰酸钾溶液中 | 溶液紫红色褪去 | SO2具有漂白性 |
C | 常温下铜片插入硝酸中 | 产生红棕色气体 | 常温下铜和硝酸一定产生NO |
D | 向某溶液中加入NaHCO3 | 产生白色沉淀 | 该溶液可能原来含有氢氧化钡 |
A. A B. B C. C D. D
下列实验中,对应的现象以及结论都正确的是( )
选项 | 实验 | 现象 | 结论 |
A | 向酸性KMnO4溶液中滴加H2O2溶液至过量 | 紫色消失 | H2O2在该反应中作还原剂 |
B | 溶有SO2的BaCl2溶液中通入气体X | 有白色沉淀产生 | X一定是Cl2 |
C | 向FeBr2和KSCN混合溶液中滴入少量现制氯水,再滴入CCl4混合振荡、静置 | 有机相呈红棕色,水相呈无色 | Fe2+的还原性大于Br- |
D | 铝丝用砂纸打磨后,放在冷的浓硝酸中浸泡一段时间后,放入CuSO4溶液中 | 铝丝表明变红色 | 铝可以从铜盐溶液中置换出铜 |
A. A B. B C. C D. D


 2.24 L H2O的分子数为0.1NA
2.24 L H2O的分子数为0.1NA 小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠。(夹持装置和A中加热装置已略,气密性已检验)
小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠。(夹持装置和A中加热装置已略,气密性已检验)
 GaN)同时又有氢气生成。反应中,每生成3molH2时就会放出30.8kJ的热量。
GaN)同时又有氢气生成。反应中,每生成3molH2时就会放出30.8kJ的热量。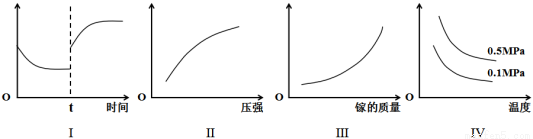
 _______;
_______; ________ (4) CH3OH________;
________ (4) CH3OH________;  ________; (6)
________; (6)  _________;
_________;