题目内容
【题目】根据要求填空:
(1)下列有关元素锗及其化合物的叙述中正确的是
A.锗的第一电离能高于碳而电负性低于碳
B.四氯化锗与四氯化碳分子都是四面体构型
C.二氧化锗与二氧化碳都是非极性的气体化合物
D.锗和碳都存在具有原子晶体结构的单质
(2)铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域.回答下列问题: ①铜原子基态电子排布式为;
②用晶体的x射线衍射法可以测得阿伏加德罗常数.对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361pm.又知铜的密度为9.00gcm﹣3 , 则镉晶胞的体积是cm3、晶胞的质量是g,阿伏加德罗常数为
(列式计算,己知Ar(Cu)=63.6);
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如图),a位置上Cl原子的杂化轨道类型为 . 已知其中一种化合物的化学式为KCuCl3 , 另一种的化学式为; 
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是 , 反应的化学方应程式为 .
【答案】
(1)BD
(2)1s22s22p63s23p63d104s1;4.7×10﹣23;4.23×10﹣22;6.01×1023mol﹣1
(3)sp3;K2CuCl3
(4)过氧化氢为氧化剂,氨与Cu2+形成配离子,两者相互促进使反应进行;Cu+H2O2 +4NH3 . H2O=[Cu(NH3)4](OH)2+4H2O
【解析】解:(1)A、碳和锗同主族,碳在第二周期,而锗在第四周期,锗是金属元素,故其第一电离能低于碳,故A错误; B、四氯化锗和四氯化碳都是分子晶体且构型相同,故B正确;
C、金属的氧化物不是气体,故C错误;
D、锗和碳都易于形成四个键,能形成原子晶体结构的单质,故D正确;
所以答案是:BD;(2)①铜是29号元素,其基态原子的电子排布式为:1s22s22p63s23p63d104s1 , 所以答案是:1s22s22p63s23p63d104s1;②1pm=10﹣10cm,故一个晶胞的体积为(361×10﹣10cm)3=4.7×10﹣23cm3;晶胞的质量=体积×密度,故一个晶胞的质量为4.7×10﹣23cm3×9.00gcm﹣3=4.23×10﹣22g;铜的晶胞为面心立方最密堆积,一个晶胞中Cu原子数目为8× ![]() +6×
+6× ![]() =4,故铜的摩尔质量=
=4,故铜的摩尔质量= ![]() ×晶胞质量×NA , 所以63.6gmol﹣1=
×晶胞质量×NA , 所以63.6gmol﹣1= ![]() ×4.23×10﹣22g×NA , 得NA=6.01×1023mol﹣1 ,
×4.23×10﹣22g×NA , 得NA=6.01×1023mol﹣1 ,
所以答案是:4.7×10﹣23;4.23×10﹣22;6.01×1023mol﹣1;(3)a位置上Cl原子成2个单键,含有2对孤对电子,杂化轨道数为4,杂化轨道类型为:sp3 ,
一种化合物的化学式为KCuCl3 , 其中铜元素为+2价,故另一种化合物中铜为+1价,CuCl3原子团的化合价为﹣2,其化学式为:K2CuCl3 , 所以答案是:sp3;K2CuCl3;(4)题中给出了两物质和铜单独不反应,而同时混合能反应,说明两者能互相促进,是两种物质共同作用的结果:其中过氧化氢为氧化剂,氨与Cu2+形成配离子,两者相互促进使反应进行,方程式可表示为:Cu+H2O2 +4NH3 . H2O=[Cu(NH3)4](OH)2+4H2O,
所以答案是:过氧化氢为氧化剂,氨与Cu2+形成配离子,两者相互促进使反应进行;Cu+H2O2 +4NH3 . H2O=[Cu(NH3)4](OH)2+4H2O.

 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案【题目】某同学进行下列实验:下列说法合理的是( )
装置 | 操作 | 现象 |
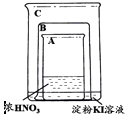
| 将盛有浓硝酸的烧杯A放入盛有淀粉KI溶液的烧杯C中,然后将铜片放入烧杯A后,立即用烧杯B罩住 | 烧杯A液体上方立即出现大量红棕色气体;一段时间后,红棕色气体消失,烧杯A和C中的液体都变成蓝色 |
A.烧杯A中发生反应:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
B.红棕色气体消失只与NO2和烧杯C中的KI发生反应有关
C.烧杯C中溶液变蓝只与NO2和C中溶液发生反应有关
D.若将铜片换成铁片,则C中的液体也可能变蓝
【题目】表为元素周期表中的一部分,列出了10种元素在元素周期表中的位置.试用元素符号、离子符号或化学式回答下列问题.
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
第2周期 | ⑥ | ⑦ | ||||||
第3周期 | ① | ③ | ⑤ | ⑧ | ⑨ | ⑩ | ||
第4周期 | ② | ④ |
(1)10种元素中,化学性质最不活泼的是(填元素符号).
(2)③④⑤三种元素最高价氧化物对应水化物中,碱性最强的是(填化学式),该物质含有的化学键类型是 .
(3)元素⑦的氢化物常温下和元素①的单质反应的化学方程式 .
(4)①和⑦两元素形成四核化合物的电子式是 .
(5)元素⑧与元素⑨相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是(填序号). a.与金属化合时,每个硫原子比每个氯原子得电子数多
b.⑨的氢化物比⑧的氢化物稳定
c.一定条件下⑧和⑨的单质都能与氢氧化钠溶液反应
d.最高价氧化物对应水化物酸性⑨比⑧强
(6)元素②的最高价氧化物的水化物与⑤的最高价氧化物的水化物反应的离子方程式为: .