题目内容
将一定质量的镁和铝混合物投入200 mL稀硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入的NaOH溶液体积的变化关系如图所示。则下列说法不正确的是( )
| A.镁和铝的总质量为9 g |
| B.合金与稀硫酸反应生成的氢气体积为10.08 L |
| C.稀硫酸的物质的量浓度为2.5 mol/L |
| D.氢氧化钠溶液的物质的量浓度为5 mol/L |
B
解析试题分析:由图像可知:将一定质量的镁和铝混合物投入200 mL稀硫酸中,固体全部溶解后,所得溶液为H2SO4、Al2(SO4)3、MgSO4的混合溶液。发生的有关化学反应方程式为:2Al+3H2SO4= Al2(SO4)3 + 3H2↑ ;Mg+ H2SO4= MgSO4+H2↑;H2SO4+2NaOH= Na2SO4+H2O。Al2(SO4)3+6NaOH= 3Na2SO4+ 2Al(OH)3↓; Mg SO4+2NaOH= Na2SO4+Mg(OH)2↓. Al(OH)3+NaOH= NaAlO2 + 2H2O. A.n(Al(OH)3) ="(0.35-0.15)mol=" 0.2mol ;n(Mg(OH)2)=" 0.15mol." m(合金)="m(Al)+m(Mg)=" 0.2mol×27g/mol+0.15mol×24g/mol=9g.正确。B.n(H2)="3/2n(Al)+" ;n(Mg)=0.45mol,所以反应放出的氢气在标准状况下的体积为V(H2)=n(H2)·Vm =0.45mol×22.4L/mol=10.08L。但选项未指明气体的条件,故体积无法确定。错误。D因为在反应Al(OH)3+NaOH= NaAlO2 + 2H2O中n(NaOH) = n(Al(OH)3)=0.2mol,V(NaOH)=40ml=0.04L,所以C(NaOH)=n/V=0.2mol÷0.04L=5mol/L.正确。C.当沉淀达到最大值时H2SO4恰好反应完全,此时的溶液为Na2SO4溶液,n(H2SO4)="1/2" n(NaOH)。V((H2SO4) ·C(H2SO4) ="1/2V(NaOH)" ·C((NaOH). 0.2L×C(H2SO4) ="1/2×0.2L×5" mol/L。解得C(H2SO4)=" 2.5" mol/L。正确。
考点:考查元素Mg、Al的单质及化合物的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案在一定条件下,将钠与氧气反应的生成物1.5g溶于水,所得溶液恰好能被80 mL浓度为0.5mol·L-1的HCl溶液中和,则生成物的成分是
| A.Na2O | B.Na2O2 | C.Na2O和Na2O2 | D.Na2O2和NaO2 |
向5.2g Fe3O4、Fe2O3、Cu的混合物中加入0.5 mol·L?1的硫酸溶液140mL时,固体恰好完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
| A.1.12g | B.6.42g | C.2.24g | D.3.24g |
硫酸亚铁溶液含有杂质硫酸铜和硫酸铁,为除去杂质,提纯硫酸亚铁,应该加入下列哪种物质
| A.锌粉 | B.镁粉 | C.铁粉 | D.铝粉 |
下列有关金属铝及其化合物的叙述正确的是
| A.铝在常温下不能与氧气反应 | B.铝不能与氯气反应 |
| C.氧化铝只能与酸反应,不能与碱反应 | D.铝既能溶于酸,又能溶于强碱 |
下列有关金属及其化合物的说法中正确的是
| A.铝和氢氧化钠溶液反应生成Al(OH)3和H2O |
B.钠在空气中燃烧生成淡黄色的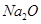 |
| C.铁在高温下与水蒸气反应生成Fe2O3和H2 |
| D.用碳酸钠和氢氧化钙反应制NaOH |
除去Na2CO3固体中少量NaHCO3的最佳方法是
| A.加入适量盐酸 | B.加热 | C.加入NaOH溶液 | D.配成溶液后通入CO2 |
下图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是( )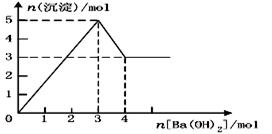
| A.NH4Al(SO4)2 | B.KAl(SO4)2 | C.Al2(SO4)3 | D.NaAlO2 |
