题目内容
将11.26 g小苏打和纯碱晶体(Na2CO3·10H2O)的混合物加热充分反应后,残留固体溶于水,配制成100 g溶液,所得Na2CO3溶液中Na2CO3的质量分数为6.36%。求:(1)原混合物中含小苏打及纯碱晶体的质量各是什么?
(2)若加热原混合物将失重多少克?
(1)原混合物中含小苏打8.4 g,纯碱晶体2.86 g。
(2)将原混合物加热失重4.9 g。
解析:2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
Na2CO3·10H2O![]() Na2CO3+10H2O
Na2CO3+10H2O
所以生成的Na2CO3与溶液中Na2CO3的质量相等。
(1)设原混合物中小苏打和纯碱晶体的质量分别是x、y。
2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
168 g 106 g
x ![]()
Na2CO3·10H2O![]() Na2CO3+10H2O
Na2CO3+10H2O
286 g 106 g
y ![]()
由题设条件可列式
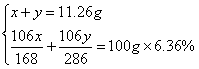
解得![]()
(2)将原混合物加热失重
Δm=11.26 g-100 g×6.36%=4.9 g

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
 CO3的质量分数为6.36%,试求:
CO3的质量分数为6.36%,试求: