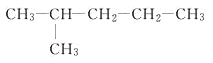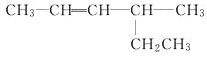题目内容
【题目】下列说法不正确的是
A. 煤的干馏和石油分馏都是物理变化
B. 石油主要是由多种烃组成的混合物
C. 石油分馏得到的汽油是混合物
D. 石油主要含有碳、氢两种元素
【答案】A
【解析】
A.煤的干馏是化学变化,石油分馏都是物理变化,故A错误;
B.石油主要是由各种烷烃、环烷烃、芳香烃组成的混合物,故B正确;
C.石油分馏得到的各种馏分是沸点在一定范围内的混合物,汽油是一种馏分,也是混合物,故C正确;
D.石油主要含有碳和氢两种元素,同时还含有少量的硫、氧、氮等元素,故D正确;
本题答案为A。

 53随堂测系列答案
53随堂测系列答案【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选用甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,判断滴定终点的现象是__________________。
(2)下列操作中可能使所测NaOH溶液的浓度偏低的是______。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,所用盐酸溶液的体积为________mL。
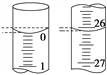
(4)某学生根据3次实验分别记录有关数据如下表:
滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.31 | 26.31 |
第二次 | 25.00 | 1.56 | a | 28.74 |
第三次 | 25.00 | 0.22 | 26.51 | b |
表格中a的数值为_________, b的数值为_________。
依据上表数据列式计算该NaOH溶液的物质的量浓度为________________。
【题目】Ⅰ、火箭升空需要高能的燃料,通常用肼(N2H4)作为燃料,N2O4做氧化剂。
(1)已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ·mol-1
2NO2(g)![]() N2O4(g) △H=-52.7kJ·mol-1
N2O4(g) △H=-52.7kJ·mol-1
试写出气态肼在四氧化二氮气体中燃烧生成氮气和气态水的热化学方程式:______________________。
(2)工业上可用次氯酸钠与过量的氨反应制备肼,该反应的氧化剂和还原剂的物质的量之比为__________________。
(3)工业上常用氨水调节溶液pH除去金属离子,常温下Cr(OH)3的溶度积Ksp=10-32,要使Cr3+浓度降至10-5mol/L,溶液pH应调至____________________
II、在130℃和180℃时,分别将0.50molCH4和a mol NO2充入1L的密闭容器中发生反应:CH4(g)+2NO2(g) ![]() N2(g)+CO2(g)+2H2O(g) △H<0,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) △H<0,测得有关数据如下表:
实验编号 | 温度 | 0min | 10min | 20min | 40min | 50min | |
1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | 0.15 |
(4)180℃时达到平衡状态时,CH4的平衡转化率为___________________。
(5)己知130℃时该反应的化学平衡常数为6.4,试计算a=__________。
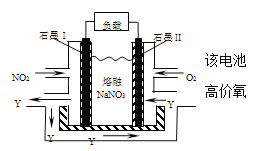
(6)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图。在使用过程中石墨I电极上生成氧化物Y (Y为氮元素最高价化化物),该电极反应为_________________。