��Ŀ����
��14�֣�ʪ����п��ұ�����̿�����ͼ���Ա�ʾ��
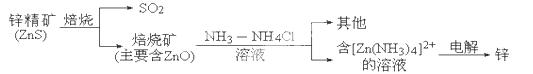
��ش��������⣺
��1����֪:N2(g)��2H2(g)===N2H4(l) ��H��a kJ��mol��1���÷�Ӧ�����Է����У���a 0(�����������������).
��2��ZnS���յķ�Ӧ2ZnS��3O2 2SO2��2ZnO���漰�������У�����������Ӧ�������� ���������Ӽ��Ļ������� .
2SO2��2ZnO���漰�������У�����������Ӧ�������� ���������Ӽ��Ļ������� .
��3��������������п�ĵ缫��ӦʽΪ___________________________.
��4��������SO2����Ba(NO3)2��Һ���գ����ֲ������Ϊ��ҵԭ�ϣ��䷴Ӧ�����ӷ���ʽΪ .
��5��п-���������﮵����ȣ����д�������ߡ��ɱ��͡�û�а�ȫ�������ŵ㡣�õ�ص��ܷ�ӦΪ2Zn��O2===2ZnO���������ҺΪKOH��Һ�����ĵ缫��ӦʽΪ ��25��ʱ���Ըõ��Ϊ��Դ����������������ͭ�����缫���500 mL 0.1mol/L CuSO4��Һ��һ��ʱ����жϵ�Դ���Ե缫���ﲢ������������缫��������Ϊ9.6 g����������Ҫ________L����(����ɱ�״��)����õ�ء�

��ش��������⣺
��1����֪:N2(g)��2H2(g)===N2H4(l) ��H��a kJ��mol��1���÷�Ӧ�����Է����У���a 0(�����������������).
��2��ZnS���յķ�Ӧ2ZnS��3O2
 2SO2��2ZnO���漰�������У�����������Ӧ�������� ���������Ӽ��Ļ������� .
2SO2��2ZnO���漰�������У�����������Ӧ�������� ���������Ӽ��Ļ������� .��3��������������п�ĵ缫��ӦʽΪ___________________________.
��4��������SO2����Ba(NO3)2��Һ���գ����ֲ������Ϊ��ҵԭ�ϣ��䷴Ӧ�����ӷ���ʽΪ .
��5��п-���������﮵����ȣ����д�������ߡ��ɱ��͡�û�а�ȫ�������ŵ㡣�õ�ص��ܷ�ӦΪ2Zn��O2===2ZnO���������ҺΪKOH��Һ�����ĵ缫��ӦʽΪ ��25��ʱ���Ըõ��Ϊ��Դ����������������ͭ�����缫���500 mL 0.1mol/L CuSO4��Һ��һ��ʱ����жϵ�Դ���Ե缫���ﲢ������������缫��������Ϊ9.6 g����������Ҫ________L����(����ɱ�״��)����õ�ء�
��1��������2��ZnS��SO2����3��Zn[��NH3��4]2++2e-=Zn+4NH3����
��4��3SO2+3Ba2++2H2O+2NO3-=3BaSO4��+2NO��+4H+����5��Zn-2e-+2OH-=ZnO+H2O�� 4.2L��
��4��3SO2+3Ba2++2H2O+2NO3-=3BaSO4��+2NO��+4H+����5��Zn-2e-+2OH-=ZnO+H2O�� 4.2L��
�����������1�����ݻ�ѧ��Ӧ������оݦ�H��T��S���������ȵ��ؼ��ٵķ�Ӧ���κ������¶������Է����У��÷�Ӧ��һ���ؼ�С�ķ�Ӧ�����Ե��÷�ӦΪ���ȷ�Ӧ��a��0ʱ���÷�Ӧ���κ������¶������Է����У���2����������ԭ��Ӧ�У�ZnS����Ԫ�صĻ��ϼ��ɡ�2�����ߵ�0�ۣ�����������Ӧ�����ý����ͷǽ���Ԫ��֮���γɵĻ�ѧ�������Ӽ�����ZnS��ZnO��SO2���ڹ��ۻ����ֻ���й��ۼ�����3�������У�������Zn[��NH3��4]2+�������Ϸ����õ��ӵĻ�ԭ��Ӧ����ⷴӦʽΪ��Zn[��NH3��4]2++2e-=Zn+4NH3������4��������������������Ժ����ᱵ��Һ֮�䷢��������ԭ��Ӧ���õ���ɫ�������ᱵ��NO���壬���ӷ���ʽΪ3SO2+3Ba2++2H2O+2NO3-=3BaSO4��+2NO��+4H+����5����п-�������ԭ��صĸ������ǽ���п����ʧ���ӵ�������Ӧ���ڼ��Ի����£��缫��ӦʽΪ��Zn-2e-+2OH-=ZnO+H2O���Ըõ��Ϊ��Դ����������������ͭ�����缫���500mL 0.1mol/L CuSO4��Һ����������Cu-2e-=Cu2+����������Cu2++2e-=Cu���Ե缫���ﲢ������������缫��������Ϊ9.6g������ٵ�ͭ�����ɵ�ͭ����4.8g��0.075mol��ת�Ƶ�����0.15mol�����ݷ�Ӧ2Zn+O2�T2ZnO����ת�Ƶ�����4molʱ������������1moL������ת�Ƶ�����0.15molʱ������������0.0375moL����������ǿ����ἰ�����֮һ���������Ŀ����������0.0375moL��5��22.4L/mol=4.2L��

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
 Mn2��+2Cl��+Cl2��+2H2O
Mn2��+2Cl��+Cl2��+2H2O ��OH��===CO
��OH��===CO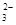 ��H2O
��H2O H��(aq)��OH��(aq)?H��0
H��(aq)��OH��(aq)?H��0 H2����Cl2��
H2����Cl2��