题目内容
【题目】下列分散系能产生丁达尔效应的是
A. 食盐水 B. 稀硫酸 C. 氢氧化钠溶液 D. 稀豆浆
【答案】D
【解析】能产生丁达尔效应的分散系是胶体,A. 食盐水属于溶液,B. 稀硫酸属于溶液,C. 氢氧化钠溶液,故A、B、C错误,D. 稀豆浆属于胶体,故D错误。答案选D。

【题目】下表是三种难溶金属硫化物的溶度积常数(25 ℃):下列有关说法中正确的是
化学式 | FeS | CuS | MnS |
溶度积 | 6.3×10-18 | 1.3×10-36 | 2.5×10-13 |
A. 25 ℃时,将CuS固体用含Mn2+的饱和溶液浸泡可溶解CuS固体
B. 25 ℃时,饱和CuS溶液中,Cu2+的浓度为1.3×10-36 mol·L-1
C. 除去某溶液中的Cu2+,可以选用FeS作沉淀剂
D. 因为H2SO4是强酸,所以反应CuSO4+H2S===CuS↓+H2SO4不能发生
【题目】碱式硫酸铁[Fe(OH)SO4]可用做净水剂、媒染剂等。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的部分工艺如下:
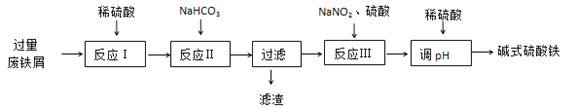
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 3.4 |
完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)反应Ⅰ中氧化还原反应的离子方程式__________________ 、 ___________________。
(2)反应Ⅱ中加入NaHCO3调节体系的pH在_____________范围内。
(3)反应Ⅲ中生成的气体遇空气变红棕色,该反应的离子方程式是_____________________。
(4)若反应Ⅲ中通入O2可减少NaNO2的用量,当消耗1molO2可节约n(NaNO2)=_____mol。
(5)用稀硫酸调节体系的pH时,若硫酸加入量过少,容易生成沉淀;若硫酸加入量过大,不利于产品形成,用化学平衡移动原理说明其原因______________________________。
(6)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)42+ 聚合离子,该水解反应的离子方程式为____________________________