题目内容
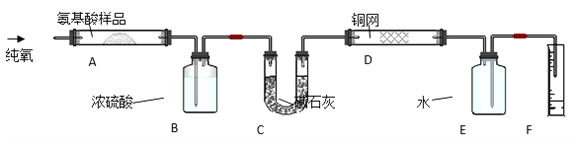
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。

请到答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是 ,其中发生反应的化学方程式为 ;
(2)实验过程中,装置B、C中发生的现象分别是 、 ,这些现象分别说明SO2具有的性质是 和 ;装置B中发生反应的离子方程式为 ;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象 ;
(4)尾气可采用 溶液吸收。
【答案】(1)蒸馏烧瓶 Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O
(2)溶液由紫色变为无色 无色溶液中出现黄色浑浊 还原性 氧化性;
2MnO4-+5SO2+2H2O═2Mn2++5SO42-+4H+
(3)品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复为红色
(4)NaOH
【解析】
试题分析:(1)装置A中盛放亚硫酸钠的仪器名称是蒸馏烧瓶;亚硫酸钠与浓硫酸反应反应生成硫酸钠、二氧化硫气体和水,反应的化学方程式为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O。
(2)高锰酸钾溶液为紫红色,具有氧化性,二氧化硫具有还原性,二者发生氧化还原反应,则观察到红色逐渐变浅直至完全褪去,二氧化硫进入硫化钠溶液中发生的氧化还原反应为2S2-+SO2+2H2O=3S↓+4OH-,则观察到出现黄色浑浊;B中S元素的化合价升高,表现还原性,C中二氧化硫中硫元素的化合价降低,表现氧化性;高锰酸钾溶液和二氧化硫气体发生的离子反应为:2MnO4-+5SO2+2H2O═2Mn2++5SO42-+4H+。
(3)因二氧化硫能使品红褪色,但加热褪色后的溶液又可恢复红色,则操作为待品红溶液完全褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,观察到的现象为无色溶液恢复为红色。
(4)尾气中含有SO2,为酸性氧化物,能与碱反应生成盐和水,所以利用氢氧化钠溶液来吸收尾气。

 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案