题目内容
化学中常用图象直观地描述化学反应的进程或结果.下列图象描述正确的是( )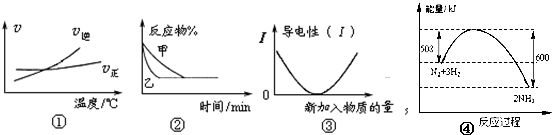

| A、根据图①可判断可逆反应 A2(g)+3B2(g)?2AB3(g) 的△H<0 | B、图②表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙压强大 | C、图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 | D、图④是N2与H2合成氨的能量变化曲线,可确定该反应1 mol N2和3 mol H2充分反应时放热一定小于92 KJ |
分析:A.升高温度,逆反应速率大于正反应速率,说明平衡向逆反应方向移动;
B.方程式中D为固体,反应物和生成物气体的计量数之和不等,则改变压强平衡移动;
C.乙酸溶液中通入氨气,生成醋酸铵,溶液导电性增强;
D.合成氨的反应为可逆反应.
B.方程式中D为固体,反应物和生成物气体的计量数之和不等,则改变压强平衡移动;
C.乙酸溶液中通入氨气,生成醋酸铵,溶液导电性增强;
D.合成氨的反应为可逆反应.
解答:解:A.升高温度,逆反应速率大于正反应速率,说明平衡向逆反应方向移动,则正反应应为放热反应,即△H<0,故A正确;
B.方程式中D为固体,反应物和生成物气体的计量数之和不等,则改变压强平衡移动,而图中平衡不移动,应为加入催化剂导致,故B错误;
C.乙酸为弱电解质,乙酸溶液中通入氨气,生成醋酸铵,溶液导电性增强,故C错误;
D.由图象可知反应热为△H=-92 KJ/mol,合成氨的反应为可逆反应,则反应1 mol N2和3 mol H2充分反应时放热一定小于92 KJ,故D正确.
故选AD.
B.方程式中D为固体,反应物和生成物气体的计量数之和不等,则改变压强平衡移动,而图中平衡不移动,应为加入催化剂导致,故B错误;
C.乙酸为弱电解质,乙酸溶液中通入氨气,生成醋酸铵,溶液导电性增强,故C错误;
D.由图象可知反应热为△H=-92 KJ/mol,合成氨的反应为可逆反应,则反应1 mol N2和3 mol H2充分反应时放热一定小于92 KJ,故D正确.
故选AD.
点评:本题考查较为综合,涉及影响化学平衡的因素、弱电解质的电离以及可逆反应,综合考查学生的分析能力,为高考常见题型,注意把握图象曲线的变化趋势,难度不大.

练习册系列答案
相关题目