题目内容
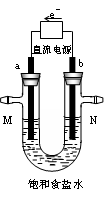
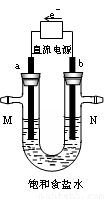
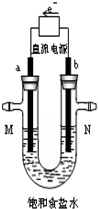 如图所示是电解氯化钠溶液(含酚酞)的部分装置.两电极均是惰性电极.
如图所示是电解氯化钠溶液(含酚酞)的部分装置.两电极均是惰性电极.(1)电解过程中阴极附近可观察到的现象为
(2)确定N出口的气体最简单的实验方法是
(3)电解的总反应离子方程式为
(4)若开始时将b电极换成铁作电极,电解液仍为NaCl溶液,写出在电解过程中U型管底部出现的现象
(5)若更换电解液用电极,将该装置用于电解精炼铜,则a电极的材料为
分析:(1)先根据电子流向判断电源的正负极,根据电源的正负极判断阴极确定现象;
(2)根据氯气的检验方法判断;
(3)根据反应物、产物写出相应的电解方程式;
(4)先根据电极反应式判断生成物,再根据生成物的变化推断现象;
(5)根据电镀原理分析判断.
(2)根据氯气的检验方法判断;
(3)根据反应物、产物写出相应的电解方程式;
(4)先根据电极反应式判断生成物,再根据生成物的变化推断现象;
(5)根据电镀原理分析判断.
解答:解:(1)根据电子流向,连接a的是负极,连接b的是正极,所以a是阴极,b是阳极,电解氯化钠溶液时,阴极上氢离子得电子生成氢气,阴极上有电子,电子带负电荷,所以吸取氢氧根离子,阴极附近呈碱性,加入酚酞后溶液呈红色,
故答案为:有气泡产生,溶液为成红色;
(2)b是阳极,阳极上氯离子失电子生成氯气,所以N出口是氯气,氯气能置换出碘化钾中的碘,碘能使淀粉变蓝色,所以可用湿润的淀粉碘化钾检验,
故答案为:用温润的淀粉碘化钾试纸,试纸变蓝则说明是Cl2;
(3)通过以上分析知,反应物是氯化钠和水,产物是氯气、氢气、氢氧化钠,离子反应为2Cl-+2H2O
Cl2↑+H2↑+2OH-,
故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-;
(4)若将b电极换成铁作电极,铁是活泼电极,在电解氯化钠溶液时,阳极上铁失电子变成二价铁离子进入溶液,阴极上还是氢离子得电子生成氢气,随着电解的进行,溶液中有氢氧根离子产生,二价铁离子和氢氧根离子生成白色的氢氧化亚铁沉淀,白色的氢氧化亚铁不稳定,很快变成灰绿色,最终变为红褐色,
故答案为:底部有白色沉淀产生,很快变成灰绿色,最终变为红褐色;
(5)电镀法精炼铜时,粗铜为阳极,精铜为阴极,所以阳极材料是粗铜;阳极上失电子变成离子进入溶液,
因作阳极的粗铜中的铜和比铜活泼的金属都失去电子进入溶液,阴极溶液中Cu2+得到电子沉积在阴极上,所以,为阴极a电极连接纯铜,电解一段时间后,溶液中铜离子浓度在减小,
故答案为:纯铜;减小.
故答案为:有气泡产生,溶液为成红色;
(2)b是阳极,阳极上氯离子失电子生成氯气,所以N出口是氯气,氯气能置换出碘化钾中的碘,碘能使淀粉变蓝色,所以可用湿润的淀粉碘化钾检验,
故答案为:用温润的淀粉碘化钾试纸,试纸变蓝则说明是Cl2;
(3)通过以上分析知,反应物是氯化钠和水,产物是氯气、氢气、氢氧化钠,离子反应为2Cl-+2H2O
| ||
故答案为:2Cl-+2H2O
| ||
(4)若将b电极换成铁作电极,铁是活泼电极,在电解氯化钠溶液时,阳极上铁失电子变成二价铁离子进入溶液,阴极上还是氢离子得电子生成氢气,随着电解的进行,溶液中有氢氧根离子产生,二价铁离子和氢氧根离子生成白色的氢氧化亚铁沉淀,白色的氢氧化亚铁不稳定,很快变成灰绿色,最终变为红褐色,
故答案为:底部有白色沉淀产生,很快变成灰绿色,最终变为红褐色;
(5)电镀法精炼铜时,粗铜为阳极,精铜为阴极,所以阳极材料是粗铜;阳极上失电子变成离子进入溶液,
因作阳极的粗铜中的铜和比铜活泼的金属都失去电子进入溶液,阴极溶液中Cu2+得到电子沉积在阴极上,所以,为阴极a电极连接纯铜,电解一段时间后,溶液中铜离子浓度在减小,
故答案为:纯铜;减小.
点评:本题考查了电解原理,注意:电解电解质溶液时,若阳极材料是活泼金属,在阳极上金属失电子发生氧化反应,若是惰性电极作阳极,溶液中的阴离子就失电子发生氧化反应,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目