题目内容
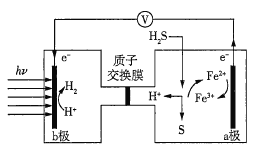
【题目】我国在太阳能光电催化-化学耦合分解硫化氢研究中获得新进展,相关装置如图所示。下列说法正确的是(已知质子交换膜只允许H+通过)( )
A.该制氢工艺中光能最终转化为化学能
B.该装置工作时,H+由b极区流向a极区
C.a极上发生的电极反应为Fe3++e-=Fe2+
D.a极区需不断补充含Fe3+和Fe2+的溶液
【答案】A
【解析】
A.该制氢工艺中光能转化为电能,最终转化为化学能,故A正确;
B.据图可知该装置工作时,H+由a极区流向b极区,在b极被还原生成氢气,故B错误;
C.a极上有电子流出,发生氧化反应,所以a极上发生的电极反应为Fe2+-e-=Fe3+,故C错误;
D.由图可知,a极区Fe3+和Fe2+可相互转化,故不需补充含Fe3+和Fe2+的溶液,故D错误;
故答案为A。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目