题目内容
下列叙述正确的是
A.液态HC1不能导电,所以HC1是非电解质
B.酸性氧化物一定是非金属氧化物
C.在水溶液中能电离产生H的化合物不定是酸
D.盐、碱一定含有金属元素
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案用硫酸酸化的草酸(H2C2O4,二元弱酸)溶液能将KMnO4溶液中的MnO4﹣转化为Mn2+。某化学小组研究发现,少量MnSO4可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,请完成以下实验设计表。
实验 编号 | 温度 | 初始pH | 0.1mol/L 草酸溶液/mL | 0.01mol/L KMnO4溶的
| 蒸馏水 体积/mL | 待测数据(反应混合液褪色 时间/s) |
① | 常温 | 1 | 20 | 50 | 30[ | t1 |
② | 常温 | 2 | 20 | 50 | 30 | t2 |
③ | 常温 | 2 | 40 | a | b | t3 |
表中a、b的值分别为:a= 、b=
(2)该反应的离子方程式 。
(3)若t1<t2,则根据实验①和②得到的结论是 。
(4)请你设计实验④验证MnSO4对该反应起催化作用,完成下表中内容.
实验方案(不 | 预期实验结果和结论 |
若反应混合液褪色时间小于实验①中的t1,则MnSO4对该反应起催化作用(若褪色时间相同,则MnSO4对该反应无催化作用) |
(5)某化学小组用滴定法测定KMnO4溶液物质的量浓度:取W g草酸晶体(H2C2O4•2H2O,其摩尔质量126 g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定两次,平均消耗KMnO4溶液V mL.请回答下列问题:
① 该测定方法中 (填“需要”或“不需要”)加入指示剂;
② 计算得KMnO4溶液的c(KMnO4)= mol/L.(请写出最后化简结果)


 体积/mL
体积/mL 要求写出具体操作过程)
要求写出具体操作过程) H++CH3COO-;FeCl3+3KSCN
H++CH3COO-;FeCl3+3KSCN

 平衡后, 向混合液中逐渐加入固体KCl过程中c(Fe3+)的变化趋势图。
平衡后, 向混合液中逐渐加入固体KCl过程中c(Fe3+)的变化趋势图。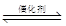 2CO2(g)+S(l)
2CO2(g)+S(l) 5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如右图,下列说法正确的是
5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如右图,下列说法正确的是