ЬтФПФкШн
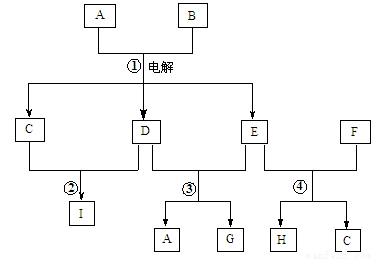
ШчЭМжаЃЌAЪЧТШЦјЕФЗЂЩњзАжУЃЌBЁЂCЪЧОЛЛЏЦјЬхЕФзАжУЃЌDжазАЬњЫПЭјЃЛЗДгІКѓEЕФЕзВПгазиЩЋЙЬЬхОлМЏЃЛFЪЧЮќЪеЖргрЦјЬхЕФзАжУЁЃ

ЃЈ1ЃЉЩЯЪізАжУжагавЛДІДэЮѓЃЌЧыжИГіЪЧ ДІЃЈгУзжФИБэЪОЃЉЁЃ
ЃЈ2ЃЉЭЈЙ§BЪЧЮЊСЫГ§ШЅ ЃЌдкBжагІМгШы ЃЛЭЈЙ§CЪЧЮЊСЫГ§ШЅ ЁЃ
ЃЈ3ЃЉаДГіDЁЂFжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪН ЁЂ ЁЃ
ЃЈ4ЃЉШчЙћAжаВњЩњТШЦј3.36LЃЈБъзМзДПіЃЉЃЌЧыМЦЫуЃК
ЂйаДГіAжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЃЌВЂБъГіAжаЕФЕчзгзЊвЦЧщПі ЁЃ
ЂкЯћКФMnO2ЕФЮяжЪЕФСП ЁЃЂлБЛбѕЛЏЕФHClЕФЮяжЪЕФСП ЁЃ
ЃЈ1ЃЉB
ЃЈ2ЃЉHCl БЅКЭЪГбЮЫЎ ЫЎеєЦј(ЫЎ) ЃЈИї1ЗжЃЉ
ЃЈ3ЃЉ2Fe+3Cl2 2FeCl3 Cl2+2NaOH=NaCl+NaClO+H2O ЃЈИї2ЗжЃЉ
2FeCl3 Cl2+2NaOH=NaCl+NaClO+H2O ЃЈИї2ЗжЃЉ
ЃЈ4ЃЉЃЈИї2ЗжЃЉ
ЂйБъЕчзгзЊвЦЕЅЯпЧХ ЫЋЯпЧХЖМПЩвдЁЃ
Ђк0.15mol Ђл0.3mol
ЁОНтЮіЁП
ЪдЬтЗжЮіЃКЃЈ1ЃЉBжаНјЦјЙмКЭГіЦјЙмгІЖдЕїЃЛЃЈ2ЃЉжЦБИЕФТШЦјжаКЌгаHClЁЂЫЎеєЦјЕШдгжЪЃЌгІЯШгУБЅКЭЪГбЮЫЎГ§ШЅHClЃЌКѓгУХЈСђЫсГ§ШЅЫЎеєЦјЃЛ
3molКЭ0.15mol ЁЃ
ПМЕуЃКПМВщЦјЬхЕФжЦБИгыаджЪгаЙиЮЪЬтЁЃ