题目内容
【题目】某小组设计如图实验,欲使甲中试管先出现浑浊,下列操作一定达不到目的的是
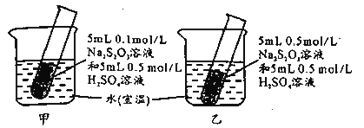
A.向甲烧杯中加入适量CaOB.向甲中试管内滴加适量浓硫酸
C.向乙烧杯中加入适量冰块D.增大甲装置所在环境的压强
【答案】D
【解析】
A项、氧化钙与水反应生成氢氧化钙放出大量的热,向甲烧杯中加入适量会使甲中反应温度高于乙,反应速率大于乙,甲中试管先出现浑浊,故A错误;
B项、向甲中试管内滴加适量浓硫酸,浓硫酸稀释时放出大量的热,溶液中氢离子浓度增大,会使反应速率加快,甲中试管先出现浑浊,故B错误;
C项、向乙烧杯中加入适量冰块,反应温度会低于甲,反应速率小于甲,甲中试管先出现浑浊,故C错误;
D项、硫代硫酸钠和硫酸都不是气体,增大甲装置所在环境的压强,不能改变反应速率,不能使甲中试管先出现浑浊,故D正确;
故选D。

练习册系列答案
相关题目