��Ŀ����
��1.8g̼����2.24L����״����O2�г��ȼ�գ���ȫ����Ӧ��ľ�����÷ų�����30.65kJ����֪��C��s��+O2��g��=CO2��g����H=��393.0kJmol-1�ۺ�������Ϣ����д��CO��ȫȼ�յ��Ȼ�ѧ����ʽ__________________________��
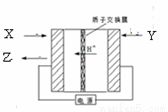
��2��������COCl2����һ����Ҫ�Ļ���ԭ�ϣ�����ũҩ��ҽҩ����������ϵ���������ҵ��ͨ��Cl2��g��+CO��g�� COCl2��g����H��0�Ʊ�����ͼ1Ϊij��ģ��ʵ���о��������ݻ�Ϊ1L���ܱ������ڸ����ʵ�Ũ����ʱ��仯�����ߣ�ͼ��Cl2����ʼŨ��Ϊ1.2mol/L��CO����ʼŨ��Ϊ1.0mol/L�����ش��������⣺
COCl2��g����H��0�Ʊ�����ͼ1Ϊij��ģ��ʵ���о��������ݻ�Ϊ1L���ܱ������ڸ����ʵ�Ũ����ʱ��仯�����ߣ�ͼ��Cl2����ʼŨ��Ϊ1.2mol/L��CO����ʼŨ��Ϊ1.0mol/L�����ش��������⣺
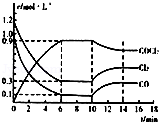
���������¶Ȳ��䣬�ڵ�8min������ϵ�е��������ʸ�1mol����ƽ��____________�ƶ������Ӧ�����������淴Ӧ����������
��������ʼͶ��Ũ�ȱ�Ϊc��Cl2��=0.8mol/L��c��CO��=0.6mol/L��c��COCl2��=____________mol/L�����ַ�Ӧ�¶Ȳ��������մﵽ��ѧƽ��ʱ��Cl2�����������������6minʱCl2�����������ͬ��
�۱Ƚϵ�8�뷴Ӧ�¶�T��8�����15min��Ӧ�¶�T��15���ĸߵͣ�T��8�� T��15���������������������=����
��3����ȼú�����е�CO2ת��Ϊ�����ѵķ�Ӧԭ��Ϊ��
2CO2��g��+6H2��g�� CH3OCH3��g��+3H2O��g��
CH3OCH3��g��+3H2O��g��
����֪һ�������£��÷�Ӧ��CO2��ƽ��ת�������¶ȡ�Ͷ�ϱ� [ ]�ı仯������ͼ2����������������ʱ������ͼ3�л���ƽ��ʱCH3OCH3�����������Ͷ�ϱ�[
]�ı仯������ͼ2����������������ʱ������ͼ3�л���ƽ��ʱCH3OCH3�����������Ͷ�ϱ�[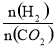 ]�仯������ͼ��
]�仯������ͼ��
��4��������,�� a mol��L -1�Ĵ��� �� b mol��L -1 Ba(OH)2 ��Һ��������,��ַ�Ӧ��,��Һ�д��� 2c(Ba 2+)=c(CH3COO-)��������Һ�д���ĵ��볣�� Ka=______________(��a��b�Ĵ���ʽ��ʾ)
ijͬѧ������þ������ʢ��NH4Cl��Һ���Թ��У��д������ݲ�����Ϊ̽���÷�Ӧԭ������ͬѧ�����������鲢�۲쵽��������ɴ˵ó��Ľ��۲��������� �� ����
ѡ�� | ʵ�鼰���� | ���� |
A | ����ʪ��ɫʯ����ֽ�����Թܿڣ���ֽ���� | ��Ӧ����NH3���� |
B | �ռ����������岢��ȼ������ʵ���ɫ | ��Ӧ����H2�� |
C | �ռ������ͬʱ�����Һ��pHΪ8.0 | ����Mg ��OH��2 |
D | ��NH4Cl��Һ�м�п��Ҳ�д������ݲ��� | ���ý����ɴٽ�NH4+ˮ�� |
������ͬѧ�ֱ�Ժ�+4����Ԫ�ص��������ʽ�����̽����
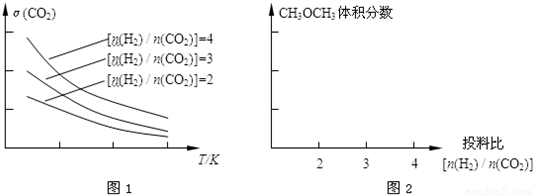
��1��������ͼװ�ý���ʵ��(�������Ѽ��飬���Ⱥͼг�װ������ȥ)��ʵ�����һ��ʱ���C��D�ж��������Եİ�ɫ�������������ΪBaSO4��

�� A�з�Ӧ�Ļ�ѧ����ʽ��______________��
��Ϊ̽��SO2��D���������ķ�Ӧ����һ��ʵ�鷢�֣�������ɫ�����Ĺ����У�D��Һ��NO3-Ũ�ȼ������䡣�ݴ˵ó����ۣ�D�г��ְ�ɫ��������Ҫԭ����__________________��
��2����������ʵ��Ժ�+4����Ԫ�ص��������ʼ�������̽����
���� | ʵ������ | ʵ������ |
1 | ȡ0.3g����Na2SO3���壬�����м���10mL 2 mol/L���ᣬ�ٵ���4��BaCl2��Һ | ������ɫ���ݣ�����BaCl2��Һ��ʼ������4 min����Һ����� |
2 | ȡ0.3g����Na2SO3���壬�����м���10mL 2 mol/L HNO3���ٵ���4��BaCl2��Һ | ������ɫ���ݣ�����BaCl2��Һ��ʼ������2 h����Һ����� |
3 | ȡ0.3g����Na2SO3���壬�����м���10mL ŨHNO3,�ٵ���4��BaCl2��Һ | ��������ɫ���壻����BaCl2��Һ����Һ��������������ɫ���� |
�������ӷ���ʽ����ʵ��1�в��������ԭ��________________��
�� ��ʵ��1��2��3�Աȣ����Եõ�����:________________��
����ͨ���������Ϸ���.Na+��ʵ��1��2�г��ֻ��ǵ�ʱ����Ӱ�죬���ǽ�һ��̽��Cl-�� NO3-�����Ӱ�죺
��� | ʵ����� | ʵ������ |
4 | ȡ____������������м���10mL2 mol /LHNO3���ٵ���4��BaCl2��Һ | ������ɫ���ݣ�������BaCl2��Һ��ʼ������20 min����Һ����� |
i.ʵ��2��4�Աȣ��һ������:C1-�Ĵ��ڿ��Լӿ���Һ��+4����Ԫ����������
ii.ʵ��I��4�Աȣ��һ������: ______________��
��ͨ������ʵ�飬��ͬѧ��Ϊ��ȷ��ij��Һ�к���SO42-��ʵ�鷽����ȡ����Һ���������ȵμ�____________ (����ĸ���)��
a��2 mol/L���ᣬ�ٵμ�BaCl2��Һ��һ��ʱ�����ְ�ɫ����
B��2 mol/L���ᣬ�ٵμ�BaCl2��Һ���������ְ�ɫ����
C��2 mol/L���ᣬ�ٵμ�BaCl2��Һ��һ��ʱ�����ְ�ɫ����
D��2 mol/L���ᣬ�ٵμ�BaCl2��Һ���������ְ�ɫ����


 ��������ӷ���ʽ ��
��������ӷ���ʽ �� ��
�� ʹ��Һ��������
ʹ��Һ��������