题目内容
下列解释实验现象的反应方程式正确的是
| A.将切开的金属Na暴露在空气中,表面由光亮逐渐变暗 2Na + O2 =Na2O2 |
B.电解氯化镁溶液产生黄绿色气体 2C1? + 2H2O Cl2↑+ H2↑+ 2OH? Cl2↑+ H2↑+ 2OH? |
| C.向AgC1悬浊液中滴加KI溶液,白色沉淀变成黄色 AgC1 + I?= AgI↓+ C1- |
D.向Ca(HCO3)2溶液中加入过量的烧碱溶液,出现白色沉淀HCO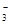 + Ca2+ + OH?= CaCO3↓ + H2O + Ca2+ + OH?= CaCO3↓ + H2O |
C
解析试题分析:A、将切开的金属Na暴露在空气中,表面由光亮逐渐变暗,主要是由于钠被氧化生成氧化钠,反应式是4Na + O2 =2Na2O,A不正确;B、电解氯化镁溶液产生黄绿色气体,同时还有氢气和氢氧化镁生成,方程式是Mg2++2C1? + 2H2O Cl2↑+ H2↑+ Mg(OH) 2↓,B不正确;C、由于碘化银的溶解度小于氯化银的,所以向AgC1悬浊液中滴加KI溶液,白色沉淀变成黄色,即反应式是AgC1 + I?= AgI↓+ C1-,C正确;D、向Ca(HCO3)2溶液中加入过量的烧碱溶液,出现白色沉淀,反应式是2HCO3-+ Ca2+ +2OH?=CaCO3↓+2H2O+CO32-,D不正确,答案选C。
Cl2↑+ H2↑+ Mg(OH) 2↓,B不正确;C、由于碘化银的溶解度小于氯化银的,所以向AgC1悬浊液中滴加KI溶液,白色沉淀变成黄色,即反应式是AgC1 + I?= AgI↓+ C1-,C正确;D、向Ca(HCO3)2溶液中加入过量的烧碱溶液,出现白色沉淀,反应式是2HCO3-+ Ca2+ +2OH?=CaCO3↓+2H2O+CO32-,D不正确,答案选C。
考点:考查金属钠的性质、电解原理的应用、溶解平衡的应用以及离子方程式的正误判断等

练习册系列答案
相关题目
下列各组物质中,物质之间不能通过一步反应就能实现图示变化的是
| 选项 | 物质转化关系 | a | b | c | d |
| A | 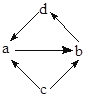 | FeCl2s | FeCl3s | Fe | CuCl2 |
| B | NO | NO2 | N2 | HNO3 | |
| C | Na2CO3 | NaOH | Na2O2 | NaHCO3 | |
| D | Al2O3 | NaAlO2 | Al | Al(OH)3 |
下列物质间的转化在给定条件下能实现的是
①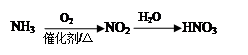
②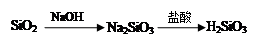
③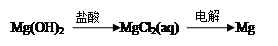
④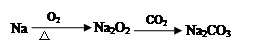
| A.②④ | B.③④ | C.①④ | D.①②③ |
向红色溶液X中通入气体Y,溶液逐渐褪色,下列对X、Y的推断正确的是
| A.若X为品红溶液,则Y可能为CO2或SO2 |
| B.若X为含酚酞的NaOH溶液,则Y可能是O3 |
| C.若X为含KSCN的FeCl3溶液,则Y一定为HI |
| D.若X为含少量KMnO4的H2SO4溶液,则Y一定为SO2 |
对下列实验的现象描述正确的是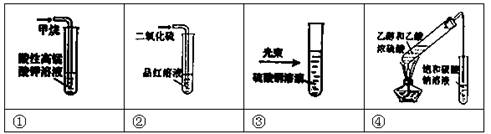
| A.实验①溶液褪色 | B.实验③溶液中看到一条光亮的通路 |
| C.实验②溶液褪色 | D.实验④饱和碳酸钠溶液下方出现油状液体 |
类比推断法是研究物质性质的常用方法之一,可预测许多物质的性质。但类比推断法是相对的,不能违背客观实际。下列说法正确的是
| A.由溶解性CaCO3<Ca(HCO3)2,则溶解性Na2CO3<NaHCO3 |
| B.向Ca(ClO)2溶液中通入少量CO2可得到CaCO3,则向Ca(ClO)2溶液中通入少量SO2可得到CaSO3 |
| C.由O2与Li加热生成Li2O,则O2与Na加热生成Na2O |
| D.有Fe与S加热生成FeS,则Cu与S加热生成Cu2S |
甲、乙、丙有如图转化关系:甲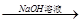 乙
乙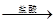 丙
丙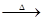 甲,甲不可能是
甲,甲不可能是
| A.A12O3 | B.SiO2 | C.NH4C1 | D.CO2 |
下列各项反应对应的图像正确的是( )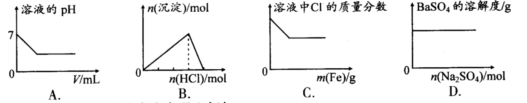
| A.25℃时,向亚硫酸溶液中通入氯气 |
| B.向NaAlO2溶液中通入HCl气体 |
| C.向少量氯化铁溶液中加入铁粉 |
| D.向BaSO4饱和溶液中加入硫酸钠 |
