题目内容
【题目】(1)磷在成键时,能将一个3s电子激发进入3d能级而参加成键,写出该激发态原子的核外电子排布式_______。
(2)钛存在两种同素异形体,![]() 采纳六方最密堆积,
采纳六方最密堆积,![]() 采纳体心立方堆积,由
采纳体心立方堆积,由![]() 转变为
转变为![]() 晶体体积______(填“膨胀”或“收缩”)
晶体体积______(填“膨胀”或“收缩”)
(3)[Cu(CH3CN)4]+是非常稳定的络合离子,配体中![]() 键和π键个数之比为_______。
键和π键个数之比为_______。
(4)水杨酸第一级电离形成离子![]() ,相同温度下,水杨酸的Ka2_________苯酚(
,相同温度下,水杨酸的Ka2_________苯酚(![]() )的Ka(填“>”“ =”或“<”)
)的Ka(填“>”“ =”或“<”)
(5)六羰基铬[Cr(CO)6]用于制高纯度铬粉,它的沸点为220![]() C。Cr(CO)6的晶体类型是_____,加热Cr(CO)6可得到高纯度铬粉和CO,反应破坏的化学键类型为_______。
C。Cr(CO)6的晶体类型是_____,加热Cr(CO)6可得到高纯度铬粉和CO,反应破坏的化学键类型为_______。
(6)已知N-N、N=N和N≡N键能之比为1.00:2.17:4.90.而C-C、C=C、C≡C键能之比为1.00:1.77:2.34.如何用这些数据理解氮分子不容易发生加成反应而乙炔容易发生加成反应?_____________。
(7)将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代可形成碳的一种新型三维立方晶体结构——T-碳。已知T-碳密度为![]() g/cm,阿伏加德罗常数为NA,则T-碳的晶胞参数a=_______pm(写出表达式即可)
g/cm,阿伏加德罗常数为NA,则T-碳的晶胞参数a=_______pm(写出表达式即可)

【答案】ls22s22p63s13p33d1 膨胀 5:2 < 分子晶体 配位键 前者每多出两条键其键能大于原来的三倍,要破坏需要吸收的能置更多;后者每增加两条化学键其键能增加量却小于原来的3倍,要破坏需要吸收的能量更少; 
【解析】
(1)磷在成键时,能将一个3s电子激发进入3d能级,P原子的3s、3p、3d上有5个未成对电子;
(2)六方堆积是最密堆积,体心立方堆积不是最密堆积;
(3) [Cu(CH3CN)4]+的配体是CH3CN,CH3CN的结构式是  ;
;
(4)![]() 中形成分子内氢键,使该微粒中酚羟基更难电离出H+;
中形成分子内氢键,使该微粒中酚羟基更难电离出H+;
(5)根据六羰基铬沸点低判断晶体类型;Cr(CO)6中Cr与CO通过配位键结合;
(6)N≡N比N-N多出2条键,其键能大于原来的三倍;C≡C比C-C多出2条键,其键能小于原来的三倍;
(7)根据![]() 计算晶胞参数a。
计算晶胞参数a。
(1)磷在成键时,能将一个3s电子激发进入3d能级,P原子的3s、3d上各有1个未成对电子,该激发态原子的核外电子排布式ls22s22p63s13p33d1;
(2)六方堆积是最密堆积,体心立方堆积不是最密堆积;所以由![]() 转变为
转变为![]() 晶体体积膨胀;
晶体体积膨胀;
(3) CH3CN的结构式是  ,单键全是
,单键全是![]() 键,三键中有1个
键,三键中有1个![]() 键、2个π键,
键、2个π键,![]() 键和π键个数之比为5:2;
键和π键个数之比为5:2;
(4)![]() 中形成分子内氢键,使该微粒中酚羟基更难电离出H+,导致该微粒酸性小于苯酚,所以相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚);
中形成分子内氢键,使该微粒中酚羟基更难电离出H+,导致该微粒酸性小于苯酚,所以相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚);
(5)六羰基铬沸点低,所以属于分子晶体;Cr(CO)6中Cr与CO通过配位键结合,Cr(CO)6分解为高纯度铬粉和CO,破坏配位键;
(6) N≡N比N-N多出两条键其键能大于原来的三倍,要破坏需要吸收的能量更多;C≡C比C-C每增加两条化学键其键能增加量却小于原来的3倍,要破坏需要吸收的能量更少,所以氮分子不容易发生加成反应而乙炔容易发生加成反应。
(7)根据均摊原则,立方金刚石晶胞中碳原子数是![]() ,T-碳中碳原子数是8×4=32,T-碳晶胞的M=8×4×12=384g/mol;
,T-碳中碳原子数是8×4=32,T-碳晶胞的M=8×4×12=384g/mol;![]() ,a=
,a= =
=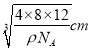 =
= pm。
pm。

 阅读快车系列答案
阅读快车系列答案