题目内容
实验室用托盘天平等仪器配制500mL 1mol·L-1的NaCl溶液,有如下操作步骤:①把称量好的NaCl晶体放人小烧杯中,加适量蒸馏水溶解;②把①所得溶液小心转人500mL容量瓶中;③继续向容量瓶中加蒸馏水至液面距离刻度l—2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部,与刻度线相切;④用少量蒸馏水洗涤烧杯和玻璃棒2—3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;⑤将容量瓶塞紧,充分摇匀。
请填写下列空白:
(1)计算需要NaCl晶体 g。
(2)实验操作步骤的正确顺序为(填序号)
(3)使用容量瓶前必须进行的一步操作是 。
(4)配制过程中,其他操作都正确,下列操作会引起浓度偏高的是 。
①未洗涤烧杯、玻璃棒②容量瓶不干燥,含有少量蒸馏水③定容时俯视标线④定容时仰视标线⑤超过刻度线,吸出一部分水;⑥摇匀后液面下降,补充水。
(5)配制上述溶液需要用到的玻璃仪器是下图中的(填编号):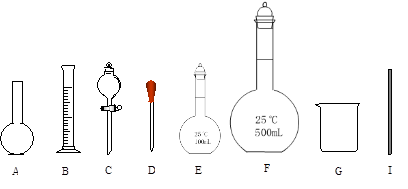
请填写下列空白:
(1)计算需要NaCl晶体 g。
(2)实验操作步骤的正确顺序为(填序号)
(3)使用容量瓶前必须进行的一步操作是 。
(4)配制过程中,其他操作都正确,下列操作会引起浓度偏高的是 。
①未洗涤烧杯、玻璃棒②容量瓶不干燥,含有少量蒸馏水③定容时俯视标线④定容时仰视标线⑤超过刻度线,吸出一部分水;⑥摇匀后液面下降,补充水。
(5)配制上述溶液需要用到的玻璃仪器是下图中的(填编号):

(1)29.25 (2)①②④③⑤ (3)验漏 (4)③ (5)BDFGI
(1)m(NaCl)= 0.5L×1mol·L-1×58.5g.mol-1=29.25g
(2)实验步骤为:a、计算m(NaCl),b、称量NaCl,c、溶解NaCl,d、冷却到室温后,将NaCl转移到500mL容量瓶中,e、洗涤刚刚溶解用过的烧杯、玻璃棒2—3次,将洗涤液一并转移到容量瓶中,f、加水定容,g、上下颠倒容量瓶,摇匀溶液;故题中顺序为:①②④③⑤;
(4)利用关系式C(NaCl)=n(NaCl)/V(溶液)分析:
①未洗涤烧杯、玻璃棒,则损失了NaCl,即n(NaCl)减小,故C(NaCl)偏低;
②容量瓶不干燥,含有少量蒸馏水,无影响;
③定容时俯视标线,则V(溶液)减小,故C(NaCl)偏高;
④定容时仰视标线,则V(溶液)增大,故C(NaCl)偏低;
⑤超过刻度线,吸出一部分水,实际上相当于V(溶液)增大,故C(NaCl)偏低;
⑥摇匀后液面下降,补充水,实际上相当于V(溶液)增大,故C(NaCl)偏低;
(5)按照实验的步骤顺序,分析所用仪器有:托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、量筒(测溶解NaCl时,所需蒸馏水的体积,可用、可不用),题目中要求玻璃仪器,故选BDFGI;
(2)实验步骤为:a、计算m(NaCl),b、称量NaCl,c、溶解NaCl,d、冷却到室温后,将NaCl转移到500mL容量瓶中,e、洗涤刚刚溶解用过的烧杯、玻璃棒2—3次,将洗涤液一并转移到容量瓶中,f、加水定容,g、上下颠倒容量瓶,摇匀溶液;故题中顺序为:①②④③⑤;
(4)利用关系式C(NaCl)=n(NaCl)/V(溶液)分析:
①未洗涤烧杯、玻璃棒,则损失了NaCl,即n(NaCl)减小,故C(NaCl)偏低;
②容量瓶不干燥,含有少量蒸馏水,无影响;
③定容时俯视标线,则V(溶液)减小,故C(NaCl)偏高;
④定容时仰视标线,则V(溶液)增大,故C(NaCl)偏低;
⑤超过刻度线,吸出一部分水,实际上相当于V(溶液)增大,故C(NaCl)偏低;
⑥摇匀后液面下降,补充水,实际上相当于V(溶液)增大,故C(NaCl)偏低;
(5)按照实验的步骤顺序,分析所用仪器有:托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、量筒(测溶解NaCl时,所需蒸馏水的体积,可用、可不用),题目中要求玻璃仪器,故选BDFGI;

练习册系列答案
相关题目