��Ŀ����
�״���һ�ֿ�������Դ�����й����Ŀ�����Ӧ��ǰ������ҵ�Ͽɲ��������Ͷ�����̼��220��280��ʹ�����Cu0-Zn0-Al2O3�������ºϳɼ״�����CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49.1kJ/mol-1�����ͬʱ��������Ӧ��CO2��g��+H2��g��?CO��g��+H2O��g����H=+41.1kJ/mol-1������˵����ȷ���ǣ�������
������A���ϳɼ״��ķ�ӦΪ���ȷ�Ӧ��
B�����������������ٽ�������̼��ת����
C��������״�����Ӧ�����ƶ���
D�����������³���He��g���������ʵ�Ũ�Ȳ��䣬��Ӧ���ʲ��䣮
B�����������������ٽ�������̼��ת����
C��������״�����Ӧ�����ƶ���
D�����������³���He��g���������ʵ�Ũ�Ȳ��䣬��Ӧ���ʲ��䣮
����⣺A���ϳɼ״��ķ�ӦΪ���ȷ�Ӧ���������¶�ƽ�������ƶ��������²����úϳɼ״�����B����
B�����������������ٽ�������̼��ת���������H2��CO2�����ʵ���֮�ȣ������CO2��ת���ʣ���B��ȷ��
C��������״�����Ӧ�����ƶ����״��IJ�������C����
D�����������³���He��g���������ʵ�Ũ�Ȳ��䣬��Ӧ���ʲ��䣬ƽ�ⲻ�ƶ���ת���ʲ��䣬��D����
��ѡB��
B�����������������ٽ�������̼��ת���������H2��CO2�����ʵ���֮�ȣ������CO2��ת���ʣ���B��ȷ��
C��������״�����Ӧ�����ƶ����״��IJ�������C����
D�����������³���He��g���������ʵ�Ũ�Ȳ��䣬��Ӧ���ʲ��䣬ƽ�ⲻ�ƶ���ת���ʲ��䣬��D����
��ѡB��
���������⿼��Ӱ�컯ѧƽ���ƶ������أ�ע�ⷴӦ���ʲ���ƽ�ⲻ�ƶ���ѡ��DΪ�����ѵ㣬�����¶ȡ�Ũ�ȶ�ƽ���Ӱ�켴�ɽ����Ŀ�ѶȲ���

��ϰ��ϵ�д�
 Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д� �����ÿ�ʱѵ��ϵ�д�
�����ÿ�ʱѵ��ϵ�д� ��Ԫȫ��������ϵ�д�
��Ԫȫ��������ϵ�д� �»ƸԱ����ܾ�ϵ�д�
�»ƸԱ����ܾ�ϵ�д�
�����Ŀ
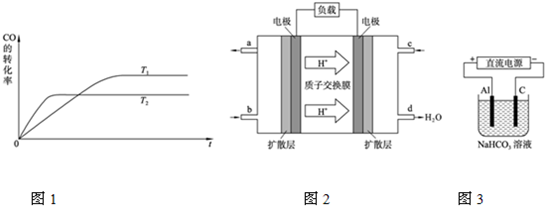
 ��Դ��ȱ���������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��Դ��ȱ���������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ���� ��2012?������һģ����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��2012?������һģ����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����