题目内容
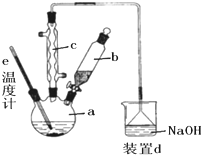
用滴管将新制的饱和氯水慢慢滴入含酚酞的NaOH稀溶液中.当滴到最后一滴时红色突然褪去.试回答下列问题:
(1)实验室保存饱和氯水的方法是______.
(2)请写出新制饱和氯水中含有氯元素的物质的化学式______.
(3)产生上述现象的原因可能有两种(简要文字说明):①是由于______;②是由于______.
简述怎样用实验证明红色褪去的原因是①或者②?
______.
(1)实验室保存饱和氯水的方法是______.
(2)请写出新制饱和氯水中含有氯元素的物质的化学式______.
(3)产生上述现象的原因可能有两种(简要文字说明):①是由于______;②是由于______.
简述怎样用实验证明红色褪去的原因是①或者②?
______.
(1)氯水是液体,应用细口瓶盛装;氯水中HClO光照易分解,所以应用棕色瓶盛放可装在棕色瓶中保存在阴凉、黑暗处,
故答案为:装在棕色瓶中保存在阴凉、黑暗处;
(2)氯气与水反应,发生Cl2+H2O=HCl+HClO,新制饱和氯水中含有氯元素的物质为HCl、HClO、Cl2,
故答案为:HCl、HClO、Cl2;
(3)氢氧化钠酚酞溶液呈红色,向其中加入新制氯水,红色褪去,原因可能为:①酚酞被强氧化剂HClO氧化而破坏;②NaOH被氯水中的酸性物质中和,红色褪去,证明褪色的原因向所得溶液中再滴入几滴NaOH溶液,若溶液又恢复成红色,原因②对;若无变化,原因①对,
故答案为:酚酞被强氧化剂HClO氧化而破坏;NaOH被氯水中的酸性物质中和,红色褪去;向所得溶液中再滴入几滴NaOH溶液,若溶液又恢复成红色,原因②对,若无变化原因①对.
故答案为:装在棕色瓶中保存在阴凉、黑暗处;
(2)氯气与水反应,发生Cl2+H2O=HCl+HClO,新制饱和氯水中含有氯元素的物质为HCl、HClO、Cl2,
故答案为:HCl、HClO、Cl2;
(3)氢氧化钠酚酞溶液呈红色,向其中加入新制氯水,红色褪去,原因可能为:①酚酞被强氧化剂HClO氧化而破坏;②NaOH被氯水中的酸性物质中和,红色褪去,证明褪色的原因向所得溶液中再滴入几滴NaOH溶液,若溶液又恢复成红色,原因②对;若无变化,原因①对,
故答案为:酚酞被强氧化剂HClO氧化而破坏;NaOH被氯水中的酸性物质中和,红色褪去;向所得溶液中再滴入几滴NaOH溶液,若溶液又恢复成红色,原因②对,若无变化原因①对.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
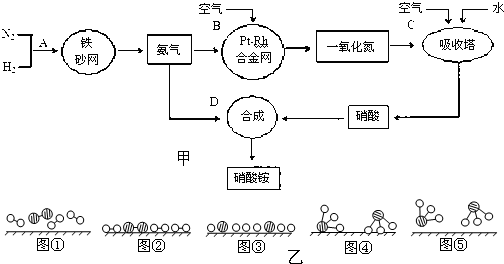
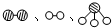 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______、______.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______、______.