题目内容
山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊--运城盐池,该湖水含盐量极高,入冬后随着温度的变化,该盐湖中会析出不同的物质,水温在10℃左右开始析出NaCl,在0℃时才开始析出MgSO4.某学生对此产生了疑问:根据下表,在10℃时MgSO4的溶解度比NaCl的溶解度小,为什么却是NaCl先析出?下列对此现象的解释最恰当的是
| 温度 | 0℃ | 10℃ | 20℃ | 30℃ |
| MgSO4的溶解度(单位:g) | 22 | 28.2 | 33.7 | 38.9 |
| NaCl的溶解度(单位:g) | 35.7 | 35.8 | 35.9 | 36.1 |
- A.硫酸镁的溶解度随温度升高而增大
- B.氯化钠的溶解度受温度影响较小
- C.盐湖中氯化钠的浓度大于硫酸镁的浓度
- D.硫酸镁的溶解度受温度影响的程度大于氯化钠的溶解度受温度影响的程度
C
分析:影响物质结晶析出有两个条件,一是物质溶解度大小,通过改变温度,使物质析出;二是溶剂的多少,通过蒸发溶剂使物质析出.
解答:物质是否结晶析出不仅与某温度下物质的溶解度有关,而且还与溶液中该物质的浓度有关.尽管MgSO4的溶解度小,但是湖水中MgSO4的含量少,溶液是不饱和的,在10℃时不会析出,只有继续降温,减小其溶解度.才有可能析出,所以在0℃时才开始析出.
所以原因是:盐湖中氯化钠的浓度大于硫酸镁的浓度.
故选C.
点评:本题主要考查了海水晒盐的原理,以及物质结晶与溶解度的关系,难度中等,概念性强,要多加分析,学会用概念解题.
分析:影响物质结晶析出有两个条件,一是物质溶解度大小,通过改变温度,使物质析出;二是溶剂的多少,通过蒸发溶剂使物质析出.
解答:物质是否结晶析出不仅与某温度下物质的溶解度有关,而且还与溶液中该物质的浓度有关.尽管MgSO4的溶解度小,但是湖水中MgSO4的含量少,溶液是不饱和的,在10℃时不会析出,只有继续降温,减小其溶解度.才有可能析出,所以在0℃时才开始析出.
所以原因是:盐湖中氯化钠的浓度大于硫酸镁的浓度.
故选C.
点评:本题主要考查了海水晒盐的原理,以及物质结晶与溶解度的关系,难度中等,概念性强,要多加分析,学会用概念解题.

练习册系列答案
相关题目
山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊--运城盐池,该湖水含盐量极高,入冬后随着温度的变化,该盐湖中会析出不同的物质,水温在10℃左右开始析出NaCl,在0℃时才开始析出MgSO4.某学生对此产生了疑问:根据下表,在10℃时MgSO4的溶解度比NaCl的溶解度小,为什么却是NaCl先析出?下列对此现象的解释最恰当的是( )
|
 Ⅰ山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊--运城盐池.
Ⅰ山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊--运城盐池.
(1)该湖水含盐量极高,但其中不可能大量存在的是______
A、NaClB、NNO3C、CaCO3D、Na2SO4
(2)一年四季,盐湖变换着不同的景色.春、秋两季碧波万顷,湖水清澈;夏季气温高达42℃,水位下降,生长的藻类使湖水变成了红色;冬季湖面上盐花丛生,洁白如雪.上述景色变换中包含的过程有______(填序号).
①蒸发; ②蒸馏; ③结晶; ④升华; ⑤溶解
Ⅱ阅读、分析下列两个材料:
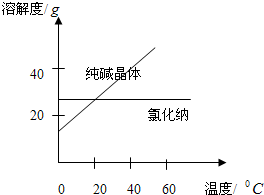
材料一:读图
材料二:
| 物质 | 熔点/℃ | 沸点/℃ | 密度g?cm-3 | 溶解性 |
| 乙二醇C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水 和乙醇 |
| 丙三醇C3H8O3 | 17.9 | 290 | 1.26 | 能跟水、酒 精以任意比 互溶 |
A、蒸馏法 B、萃取法 C、“溶解、结晶、过滤”的方法 D、分液法
(1)将纯碱从氯化纳和纯碱的混合物中分离出来,最好应用______.
(2)将乙二醇和丙三醇相互分离的最佳方法是______.
(3)用CCl4提取溴水中的溴单质的最佳方法是______.
(4)分离汽油和水的最佳方法是______.
Ⅰ山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊--运城盐池.
(1)该湖水含盐量极高,但其中不可能大量存在的是______
A、NaClB、NNO3C、CaCO3D、Na2SO4
(2)一年四季,盐湖变换着不同的景色.春、秋两季碧波万顷,湖水清澈;夏季气温高达42℃,水位下降,生长的藻类使湖水变成了红色;冬季湖面上盐花丛生,洁白如雪.上述景色变换中包含的过程有______(填序号).
①蒸发; ②蒸馏; ③结晶; ④升华; ⑤溶解
Ⅱ阅读、分析下列两个材料:
材料一:读图
材料二:
根据上述材料及课本知识,回答下列问题(填写序号):
A、蒸馏法 B、萃取法 C、“溶解、结晶、过滤”的方法 D、分液法
(1)将纯碱从氯化纳和纯碱的混合物中分离出来,最好应用______.
(2)将乙二醇和丙三醇相互分离的最佳方法是______.
(3)用CCl4提取溴水中的溴单质的最佳方法是______.
(4)分离汽油和水的最佳方法是______.
(1)该湖水含盐量极高,但其中不可能大量存在的是______
A、NaClB、NNO3C、CaCO3D、Na2SO4
(2)一年四季,盐湖变换着不同的景色.春、秋两季碧波万顷,湖水清澈;夏季气温高达42℃,水位下降,生长的藻类使湖水变成了红色;冬季湖面上盐花丛生,洁白如雪.上述景色变换中包含的过程有______(填序号).
①蒸发; ②蒸馏; ③结晶; ④升华; ⑤溶解
Ⅱ阅读、分析下列两个材料:
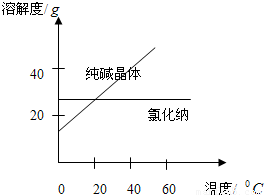
材料一:读图
材料二:
| 物质 | 熔点/℃ | 沸点/℃ | 密度g?cm-3 | 溶解性 |
| 乙二醇C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水 和乙醇 |
| 丙三醇C3H8O3 | 17.9 | 290 | 1.26 | 能跟水、酒 精以任意比 互溶 |
A、蒸馏法 B、萃取法 C、“溶解、结晶、过滤”的方法 D、分液法
(1)将纯碱从氯化纳和纯碱的混合物中分离出来,最好应用______.
(2)将乙二醇和丙三醇相互分离的最佳方法是______.
(3)用CCl4提取溴水中的溴单质的最佳方法是______.
(4)分离汽油和水的最佳方法是______.

 Ⅰ山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊--运城盐池.
Ⅰ山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊--运城盐池.