题目内容
下列反应的离子方程式,正确的是( )。
| A.碳酸氢钠和烧碱溶液:HCO3-+OH-=CO32-+H2O |
| B.石灰水中通入过量的CO2: CO2+Ca2++2OH-=CaCO3↓+H2O |
| C.稀硫酸和氢氧化钡:Ba2++SO42-=BaSO4↓ |
| D.氯化铁溶液和氨水:Fe3++3OH-=Fe(OH)3↓ |
A
解析试题分析:B、石灰水中通入过量的CO2,生成的是Ca(HCO3)2,离子方程式是CO2+OH-=HCO3-+H2O; C、稀硫酸和氢氧化钡:除了Ba2++SO42-=BaSO4↓外还有H++OH-= H2O,所以离子方程式为Ba2++SO42-+2H++2OH-= BaSO4↓+2H2O;D、氯化铁溶液和氨水反应,氨水是弱电解质,不能拆成离子形式Fe3++ 3NH3。H2O =Fe(OH)3↓+ 3NH4+。
考点:离子方程式的书写注意问题。

练习册系列答案
相关题目
下列关于电解质、非电解质的说法正确的是
| A.氯气溶于水得氯水,该溶液能导电,因此氯气是电解质 |
| B.CaCO3饱和溶液导电能力很弱,故CaCO3是弱电解质 |
| C.导电能力弱的溶液肯定是弱电解质的溶液 |
| D.HF的水溶液中既有H+、F-,又有大量的HF分子,因此HF是弱电解质 |
下列离子方程式正确的是
| A.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O |
| B.钠与水的反应Na+2H2O=Na++2OH-+ H2 ↑ |
| C.硫酸氢钠溶液与少量氢氧化钡溶液混合:2H++SO42-+ Ba2++2OH-= BaSO4↓+2H2O |
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
下列物质的分类组合全部正确的是
| 编组 | 强电解质 | 弱电解质 | 非电解质 |
| A | NaCl | H2O | Cl2 |
| B | H2SO4 | CaCO3 | CCl4 |
| C | HCl | HClO | 氨水 |
| D | Ba(OH)2 | CH3COOH | C2H5OH |
在某无色透明的酸性溶液中,能共存的离子组是( )
| A.Na+、K+、SO42-、CO32- | B.Na+、K+、Cl-、NO3- |
| C.Cu2+、K+、SO42-、NO3- | D.Ba2+、K+、SO42-、Cl- |
下列物质水溶液能导电,但该物质属于非电解质的是
| A.Na2O | B.Cl2 | C.H2SO4 | D.SO2 |
只能表示某一个化学反应的离子方程式的是
| A.H++OH-=H2O |
| B.CO32-+2H+=H2O+CO2↑ |
| C.Cu(OH)2+2H+=Cu2++2H2O |
| D.Cu2++2OH-+Ba2++SO42-=BaSO4↓ +Cu(OH)2↓ |
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL1mol·L-1的HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法正确的是( )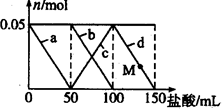
A.b曲线表示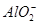 的减少,d曲线表示氢氧化铝的溶解 的减少,d曲线表示氢氧化铝的溶解 |
| B.b和c曲线表示的离子反应是相同的 |
| C.M点时Al(OH)3的质量小于3.9g |
D.原混合溶液中的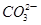 与 与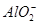 的物质的量之 的物质的量之 |
下列各组离子能在溶液中大量共存的是
| A.K+、H+、SO42-、OH- | B.Na+、Ca2+、CO32-、NO3- |
| C.Na+、H+、C1-、CO32- | D.Na+、Cu2+、C1-、SO42- |