题目内容
【题目】下表为元素周期表的一部分,请回答有关问题
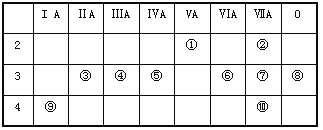
(1)⑤和⑧的元素符号是_______和_______。
(2)表中最活泼的金属元素是___________,非金属性最强的元素是___________(填写元素符号)。
(3)表中能形成两性氢氧化物的元素是___________,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的化学方程式:__________________;__________________。
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:_________________________。
【答案】(1)Si;Ar(2)K;F
(3)Al;2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O;Al(OH)3+KOH= KAlO2+2H2O
(4)将⑦单质(Cl2)通入盛有⑩的钠盐(NaBr)溶液中,加入CCl4 看四氯化碳层是否呈红棕色,若呈红棕色,则说明⑦(Cl2)的氧化性大于⑩(Br 2)的氧化性
【解析】试题(1)⑤和⑧的元素符号是Si和Ar。
(2)同周期元素从左到右金属性减弱、非金属性增强;同主族元素从上到下金属性增强、非金属性减弱,表中最活泼的金属元素是K,非金属性最强的元素是F。
(3)表中能形成两性氢氧化物的元素是Al,氢氧化铝与硫酸、氢氧化钾反应的化学方程式:2Al(OH)3 + 3H2SO4 = Al2(SO4)3 + 6H2O ;Al(OH)3 + KOH = KAlO2 + 2H2O。
(4)氧化剂的氧化性大于氧化产物的氧化性, Cl2通入盛有NaBr溶液中,加入CCl4 看四氯化碳层是否呈红棕色,若呈红棕色,则说明Cl2的氧化性大于Br 2的氧化性。

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目