题目内容
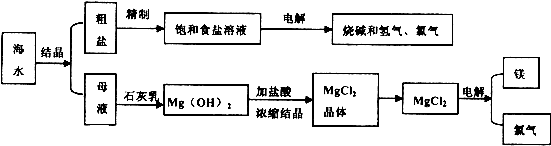
(12分)海水是取之不尽用之不竭的化学资源,从海水中可提取多种化工原料,下图是某化工厂对海水资源综合利用的示意图。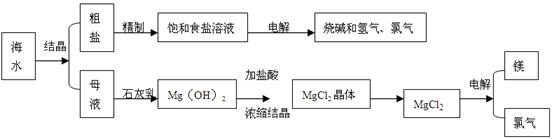
(1)请写出电解食盐水的化学方程式
(2)母液中含有K+、Na+ 、Mg2+等阳离子,从图中可看出对母液进行一系列的加工可制得金属镁。
①石灰乳是生石灰与水作用形成的化合物,从充分利用当地海洋化学资源,提高生产与经济效益的角度考虑,生产生石灰的主要原料是
②电解熔融氯化镁的化学方程式是
③电解无水氯化镁所得的镁蒸气在特定的环境里冷却后可得固态的金属镁,下列物质中可以用作镁蒸气的冷却剂的是(填写代号)
A. H2 B. CO2 C.空气 D. Ar
(3)在该化工厂中,海水提取氯化钠后的母液经过提取氯化镁后又形成了新的母液,向新母液中加入氯气,又制取了重要的化工原料溴单质
①生成溴单质的化学反应的离子方程式是 ,其中氧化剂是
工业生产中将溴单质从混合物中分离出来应采用 (填实验方法)
②以下是对生产溴单质所用的氯气寻找货源的设想,其中合理的是 (填写代号)
A.从外地购买 B.在当地新建生产厂
C.从本厂生产烧碱处循环 D.从本厂生产镁单质处循环
(1)2NaCl+2 H2O 2NaOH+ H2 ↑+Cl2 ↑
2NaOH+ H2 ↑+Cl2 ↑
(2)①贝壳 ②MgCl2 Mg +Cl2 ↑ ③AD
Mg +Cl2 ↑ ③AD
(3)①2Br-+ Cl2=Br2+2Cl-, 萃取 ②CD
解析试题分析:(1)电解食盐水得到NaOH、氢气、氯气,是氯碱工业的主要化学反应,要熟记;
(2)①要充分利用当地海洋化学资源,提高生产与经济效益,考虑海边上大量的贝壳主要成分是碳酸钙,使其高温分解可制得生石灰;②电解熔融氯化镁生成镁单质与氯气;③注意可用作镁蒸气的冷却剂不能和镁发生反应,所以选择AD;
(3)①新的母液中含有Br-,通入氯气可以把Br-氧化得到溴单质,此时溴溶在水中,可以用有机溶剂进行萃取使溴分离出来;②氯气的货源可从氯碱工业产物和电解氯化镁产物考虑。
考点:考查海水资源的综合利用
点评:熟悉海水综合利用的方法,熟悉常见物质的性质

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案