题目内容
12.加入水中得到溶液显酸性的物质是( )| A. | Na2O | B. | NO2 | C. | H2 | D. | SiO2 |
分析 A、盐溶于水生成氢氧化钠,溶液显碱性;
B、二氧化氮溶于水生成硝酸和一氧化氮,溶液显酸性;
C、氢气不溶于水;
D、二氧化硅不溶于水.
解答 解:A、盐溶于水生成氢氧化钠,Na2O+H2O=2NaOH,溶液显碱性,故A错误;
B、二氧化氮溶于水生成硝酸和一氧化氮,3NO2+H2O=2HNO3+NO,溶液显酸性,故B正确;
C、氢气不溶于水,溶液呈中性,故C错误;
D、二氧化硅不溶于水,溶液呈中性,故D错误;
故选B.
点评 本题考查了物质性质的分析应用,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
2.进行化学实验必须注意安全,下列说法不正确的是( )
| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌 | |
| D. | 金属钠着火,立即用水扑灭 |
20.锌与100mL 18.5mol•L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6L(标准状况).将反应后的溶液稀释至1L,测得溶液的pH=1.下列叙述正确的是.( )
| A. | 反应中共消耗1.85 mol H2SO4 | B. | 气体甲中SO2与H2的体积比为1:4 | ||
| C. | 反应中共消耗65 g Zn | D. | 反应中共转移3.6 mol电子 |
7.半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂.实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)
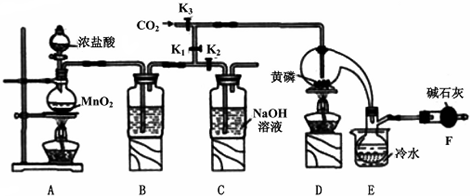
已知黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5.PCl3遇水会强烈水解生成H3PO3和HCl;遇O2会生成POCl3,POCl3溶于PCl3.PCl3、POCl3的熔沸点见下表:
请回答下列问题:
(1)A装置中制氯气的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;加热\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)B中所装试剂是浓H2SO4,F中碱石灰的作用是吸收多余的氯气,防止空气中的水汽进入烧瓶与PC13反应.
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(4)粗产品中常含有POC13、PCl5等.加入黄磷加热除去PCl5后.通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.

已知黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5.PCl3遇水会强烈水解生成H3PO3和HCl;遇O2会生成POCl3,POCl3溶于PCl3.PCl3、POCl3的熔沸点见下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)A装置中制氯气的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;加热\;}}{\;}$Mn2++Cl2↑+2H2O.
(2)B中所装试剂是浓H2SO4,F中碱石灰的作用是吸收多余的氯气,防止空气中的水汽进入烧瓶与PC13反应.
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(4)粗产品中常含有POC13、PCl5等.加入黄磷加热除去PCl5后.通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
17.下列有机反应属于加成反应的是( )
| A. | HC≡CH+HCl$\stackrel{催化剂}{→}$H2C=CHCl | |
| B. | C 2H5OH+CH3COOH$→_{△}^{浓硫酸}$CH3COOC2H5+H2O | |
| C. | CH4+2O2 $\stackrel{点燃}{→}$ CO2+2H2O | |
| D. | 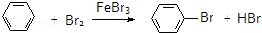 |
4.短周期主族元素X、Y、Z、W的原子序数依次增大,其中元素X的原子最外层电子数是其电子层数的2倍,元素Y在同周期的主族元素中原子半径最大,元素Z是地壳中含量最高的金属元素,W的单质是一种淡黄色固体.下列说法正确的是( )
| A. | X、Y均只有1种氧化物 | |
| B. | 原子半径:X<Y<Z | |
| C. | 简单气态氢化物的热稳定性:X>W | |
| D. | Y、Z、W的最高价氧化物的水化物能相互反应 |
1.下列叙述中,不能用平衡移动原理解释的是( )
| A. | 由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深 | |
| B. | 红棕色的NO2,加压后颜色先变深后变浅 | |
| C. | 实验室用排饱和食盐水法收集氯气 | |
| D. | 工业上利用O2与SO2反应制取SO3时通入过量O2 |
2.下列反应中,放出气体的物质的量最多的是( )
| A. | 0.1mol Fe与足量的盐酸反应 | B. | 0.4mol Cu投入到足量的稀硫酸中 | ||
| C. | 0.1mol Al与足量的NaOH溶液反应 | D. | 0.1mol Fe与足量的水反应 |