题目内容
写出下列反应的热化学方程式:
(1)10g乙烷(C2H6)气体完全燃烧生成液态水放出热量520kJ.
(2)10gCaCO3高温分解吸收热量17.56kJ.
(1)10g乙烷(C2H6)气体完全燃烧生成液态水放出热量520kJ.
(2)10gCaCO3高温分解吸收热量17.56kJ.
(4分,每小题2分)
(1)2C2H6(g) + 7O2(g) = 4CO2(g) + 6H20(l); △H=-3120kJ/mol;
(2)CaCO3(s) = CaO(s) + CO2(g); △H=+175.6kJ/mol。
(1)2C2H6(g) + 7O2(g) = 4CO2(g) + 6H20(l); △H=-3120kJ/mol;
(2)CaCO3(s) = CaO(s) + CO2(g); △H=+175.6kJ/mol。
试题分析:(1)10g乙烷(C2H6)气体完全燃烧生成液态水放出热量520kJ,那么2mol乙烷(C2H6)气体完全燃烧生成液态水放出热量3120kJ,故乙烷燃烧的化学方程式为2C2H6(g) + 7O2(g) = 4CO2(g) + 6H20(l) △H=-3120kJ/mol。
(2)10gCaCO3高温分解吸收热量17.56kJ,那么1molCaCO3高温分解吸收热量175.6kJ,故CaCO3高温分解的热化学方程式为CaCO3(s) = CaO(s) + CO2(g); △H=+175.6kJ/mol。
点评:本题主要考查了热化学方程式的书写,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比。

练习册系列答案
相关题目



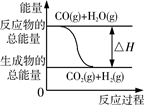
 CO2(g)+H2(g)的△H大于0
CO2(g)+H2(g)的△H大于0 与
与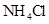 的反应
的反应