题目内容
根据下列五种元素的电离能数据(单位:kJ·mol-1),回答下面问题。
元素代号 | I1 | I2 | I3 | I4 |
Q | 2 080 | 4 000 | 6 100 | 9 400 |
R | 500 | 4 600 | 6 900 | 9 500 |
S | 740 | 1 500 | 7 700 | 10 500 |
T | 580 | 1 800 | 2 700 | 11 600 |
U | 420 | 3 100 | 4 400 | 5 900 |
(1)在周期表中,最可能处于同一族的是( )。
A.Q和R
B.S和T
C.T和U
D.R和T
E.R和U
(2)电解它们的熔融氯化物,阴极电极反应式最可能正确的是( )。
A.Q2++2e-→Q
B.R2++2e-→R
C.S3++3e-→S
D.T3++3e-→T
E.U2++2e-→U
(3)它们的氯化物的化学式,最可能正确的是( )。
A.QCl2
B.RCl
C.SCl3
D.TCl
E.UCl4
(4)下列元素中,化学性质和物理性质最像Q元素的是( )。
A.硼(1s22s22p1)
B.铍(1s22s2)
C.锂1s22s1
D.氢(1s1)
E.氦(1s2)
(1)E (2)D (3)B (4)E
【解析】五种元素的各级电离能中发生突跃式增大的情况是:R有I2?I1、S有I3?I2、T有I4?I3、U有I2?I1,化合价分别为+1、+2、+3、+1。(1)周期表中同一族的元素的最外层电子排布相同,所以它们的化合价应该是相同的(电离能发生突跃式增大的情况应相同),只有E选项符合要求,R和U均为+1价。(2)电解它们的熔融氯化物,阴极电极反应式为相应价态的阳离子得电子被还原,只有选项D正确。(3)各元素价态与化合物中氯原子数相同的只有选项B。(4)Q的第一电离能比其他元素的第一电离能明显高很多,最有可能为稀有气体或惰性金属。

 名校课堂系列答案
名校课堂系列答案工业上用粗氧化铜(含杂质FeO)为原料制取氯化铜晶体(CuCl2·2H2O)的生产流程如下:
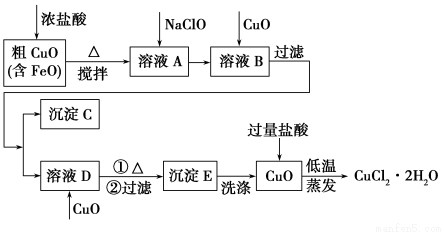
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
完全沉淀时的pH | ≥9.6 | ≥6.4 | 3~4 |
(1)写出向溶液A中加入NaClO的离子方程式___________________________________。
(2)沉淀C的化学式为________。
(3)实验室如何检验沉淀E已洗涤干净?________。
(4)低温蒸发的目的是______________________________________。
(5)流程中两次加入了CuO,而不是一次性向溶液B中加入过量的CuO,其理由是________________________________________________。
