��Ŀ����
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ٣����ڱ��е�λ�ã�
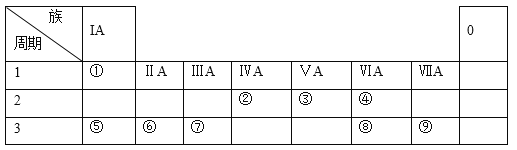
�ش��������⣺
��1��д���ڣ��ۣ��ܵ���̬�⻯����ȶ���ǿ��_______________________��
��2����-��ļ����Ӱ뾶�ɴ�С��˳��Ϊ��_______________________���������ӷ��ţ�
��3���õ���ʽ��ʾ�ڵ������������γɹ��̣�____________��
��4�������ʵ��Ƚ�Ԫ�آ���߽����Ե����ǿ����_________________��
��5�� X��Y�ɢ٢ڢ��е����ֻ�����Ԫ����ɡ�X����Һ����С�մ�Ӧ����Y����X��������ϵ������ķ��ӣ�����Է�������Ϊ46����X������Ϊ_________��д��X��Һ��С�մ�Ӧ����������ʽΪ___________________��
��6�����ɢ١�������Ԫ����ɵĿռ乹��Ϊ��������ṹ���л���A���Ԫ�صĵ��ʿ����Ƴɵ�أ������װ��KOHŨ��Һ������Ķ��Ե缫���ҽ���KOH��Һ�У��ڼ�ͨ��A���Ҽ�ͨ��ܵĵ��ʣ�����ĵ缫��ӦʽΪ��_________________________________��һ��ʱ���KOH��Ũ�Ƚ�___����������С���������䡱����ȷ��������
���𰸡� H2O>NH3>CH4 S2->Cl->Na+>Mg2+>Al3+ ![]() ȡ��С��ͬ��þ�� �������ֱ�Ͷ�뵽Ũ����ͬ��������Һ�У�þ���� Ӧ�����ң���֤�������ԣ�Mg>Al ���� HCOOH+HCO3-=HCOO-+CO2��+H2O CH4-8e-+10OH-=CO32-+7H2O ��С
ȡ��С��ͬ��þ�� �������ֱ�Ͷ�뵽Ũ����ͬ��������Һ�У�þ���� Ӧ�����ң���֤�������ԣ�Mg>Al ���� HCOOH+HCO3-=HCOO-+CO2��+H2O CH4-8e-+10OH-=CO32-+7H2O ��С
������������Ԫ�آ������ڱ��е�λ�ÿ�֪�ֱ���H��C��N��O��Na��Mg��Al��S��Cl����
��1��ͬ�����������ҷǽ���������ǿ���⻯���ȶ�������ǿ������������ܵ���̬�⻯����ȶ���ǿ��˳��ΪH2O>NH3>CH4����2�����Ӳ���Խ�࣬�����Ӱ뾶Խ���Ӳ�ṹ��ͬ�����ӣ������Ӱ뾶����ԭ�������������С���������Ӱ뾶S2->Cl->Na+>Mg2+>Al3+����3��CO2�ǹ��ۻ�����õ���ʽ��ʾ���γɹ���Ϊ![]() ����4��������Խǿ�����ᷴӦԽ���ң���Ƚ�Ԫ�آ���߽����Ե����ǿ����ʵ�鷽�������Ϊ��ȡ��С��ͬ��þ�� �������ֱ�Ͷ�뵽Ũ����ͬ��������Һ�У�þ����Ӧ�����ң���֤�������ԣ�Mg>Al����5�� X��Y�ɢ٢ڢ��е����ֻ�����Ԫ����ɡ�X����Һ����С�մ�Ӧ����Y����˵��X���ᣬY��CO2����X��������ϵ������ķ��ӣ�����Է�������Ϊ46����X������Ϊ���ᣬX��Һ��С�մ�Ӧ�����ӷ���ʽΪHCOOH+HCO3-=HCOO-+CO2��+H2O����6�����ɢ���������Ԫ����ɵĿռ乹��Ϊ��������ṹ���л���A�Ǽ��飬���Ԫ�صĵ������������Ƴɵ�أ������װ��KOHŨ��Һ������ԭ����и�������ʧȥ���ӵ�������Ӧ����缫�Ǹ������缫��ӦʽΪCH4-8e-+10OH-=CO32-+7H2O��������������̼���ƺ�ˮ������Ӧ�������������ƣ�����һ��ʱ���KOH��Ũ�Ƚ���С��
����4��������Խǿ�����ᷴӦԽ���ң���Ƚ�Ԫ�آ���߽����Ե����ǿ����ʵ�鷽�������Ϊ��ȡ��С��ͬ��þ�� �������ֱ�Ͷ�뵽Ũ����ͬ��������Һ�У�þ����Ӧ�����ң���֤�������ԣ�Mg>Al����5�� X��Y�ɢ٢ڢ��е����ֻ�����Ԫ����ɡ�X����Һ����С�մ�Ӧ����Y����˵��X���ᣬY��CO2����X��������ϵ������ķ��ӣ�����Է�������Ϊ46����X������Ϊ���ᣬX��Һ��С�մ�Ӧ�����ӷ���ʽΪHCOOH+HCO3-=HCOO-+CO2��+H2O����6�����ɢ���������Ԫ����ɵĿռ乹��Ϊ��������ṹ���л���A�Ǽ��飬���Ԫ�صĵ������������Ƴɵ�أ������װ��KOHŨ��Һ������ԭ����и�������ʧȥ���ӵ�������Ӧ����缫�Ǹ������缫��ӦʽΪCH4-8e-+10OH-=CO32-+7H2O��������������̼���ƺ�ˮ������Ӧ�������������ƣ�����һ��ʱ���KOH��Ũ�Ƚ���С��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ������������������ ��һ�ֶ�������Ͻ𣬳������л�����������ij��������Ni��Fe��Cu�������ᡢ����Һ��Ӧ�IJ��������ʣ�Ϊԭ����ȡ�ô�������Ҫ�������£�

��֪��25��ʱ����0.1mol/L�������Ӳⶨ�õ��������ݣ�
���� | CuS | Cu(OH)2 | Ni(OH)2 | NiS | Fe(OH)3 | |
Ksp | 6��10-36 | 3��10-19 | ||||
pH | ��ʼ���� | 4.7 | 7.2 | 1.9 | ||
������ȫ | 6.7 | 9.2 | 3.2 | |||
������Ϣ�ش�
��1������ٳ�����Ũ������������д�����ʱ������������Ӧ�Ļ�ѧ����ʽ__________��
��2���������Ӧ�������Ũ�ȡ��¶ȵ���������ͼ�����Ľ��������¶ȵĹ�ϵ���¶ȸ���100��ʱ��Ni2+�����ʽ��͵�ԭ�������______________��

��3����Һl�к���0.8mol/LNi2+��0.1mol/LFe3+��0.1mol/LCu2+������ڵ���������������Ҫ�ȷ������Ԫ�ء�ͭԪ�أ����Ƶ������Ϊ�ﵽ��Ŀ�ģ�Ӧ�ȼ�NaOH����Һ������_______����pH��ȡֵ��Χ�����ټ�_______��ѡ������Լ�����ţ�������Һ��Ni2+��ʼ�γ�NiSʱ��c(Cu2+)_______����������Һ����仯��
A������ B����ˮ C. A12S3 D.H2S
��4����������ɵ�Ni(CO)4��̼�Ļ��ϼ���KCN��̼�Ļ��ϼ���ͬ����Ni(CO)4��Ni�Ļ��ϼ�Ϊ______����ҵ��Ҳ����NaClO����NiSO4�����Ƶõ�NiOOH�ȷֽ����л�ԭ�õ�Ni��ClO-�ڼ�������������Ni2+����NiOOH�����ӷ���ʽΪ_____________��
��5�������Ŀ���ǽ�������������ö��״�ġ������������������Ӷ���ǿ�������������ԣ���������ӷ���ʽΪ___________________��


