��Ŀ����
��10�֣���1���ٸ���ͼʾ��д����Ӧ���Ȼ�ѧ����ʽ�� ��
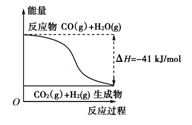
�ڸ�����ͼ��ʾ������ж�����˵������ȷ���ǣ� ��
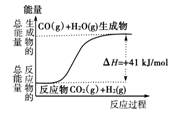
��2����֪16 g��������ȫȼ��ʱ�ų�148.4 kJ���������÷�Ӧ���Ȼ�ѧ����ʽ�� ��
��3����ͼ��ij�¶��£�N2��H2��Ӧ�����������仯������ͼ���÷�Ӧ���Ȼ�ѧ����ʽΪ�� ��
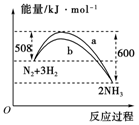
a��b�������߲��������ԭ��ܿ����� ��

�ڸ�����ͼ��ʾ������ж�����˵������ȷ���ǣ� ��

| A�����Ȼ�ѧ����ʽΪ��CO(g)��H2O(g)===CO2(g)��H2(g)������H����41 kJ/mol |
| B���÷�ӦΪ���ȷ�Ӧ |
| C���÷�ӦΪ���ȷ�Ӧ |
| D����H2OΪҺ̬ʱ���䷴Ӧ��ֵС��41 kJ/mol |
��3����ͼ��ij�¶��£�N2��H2��Ӧ�����������仯������ͼ���÷�Ӧ���Ȼ�ѧ����ʽΪ�� ��

a��b�������߲��������ԭ��ܿ����� ��
��10�֣���ÿ��2�֣�
�ٷ���ʽ�� CO��g��+H2O��g��= CO2��g��+ H2��g�� ��H = ��41 kJ/mol ��
�ڣ� BD ��
��2���Ȼ�ѧ����ʽ�� S��s��+O2��g�� = SO2��g�� ��H = ��296.8 kJ/mol��
��3���Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��= 2NH3��g�� ��H = ��92 kJ/mol��
a��bԭ��ܿ����� b���˴�
�ٷ���ʽ�� CO��g��+H2O��g��= CO2��g��+ H2��g�� ��H = ��41 kJ/mol ��
�ڣ� BD ��
��2���Ȼ�ѧ����ʽ�� S��s��+O2��g�� = SO2��g�� ��H = ��296.8 kJ/mol��
��3���Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��= 2NH3��g�� ��H = ��92 kJ/mol��
a��bԭ��ܿ����� b���˴�
��

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
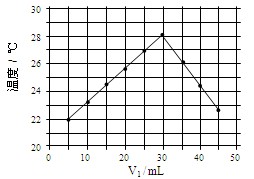
 ���һ����ѧ��Ӧ����Ӧ����������������������������ͼ��ʾ�Ĺ�ϵ����÷�Ӧ����__________��Ӧ��
���һ����ѧ��Ӧ����Ӧ����������������������������ͼ��ʾ�Ĺ�ϵ����÷�Ӧ����__________��Ӧ��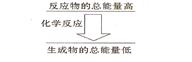
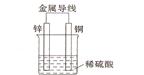
 2H2(g)+O2(g)�����Զ����������Ǹ����о�����Ҫ�ȵ㡣����Ϊ�����о�����������
2H2(g)+O2(g)�����Զ����������Ǹ����о�����Ҫ�ȵ㡣����Ϊ�����о�����������