题目内容
(2011·吉林省实验中学模考)在一定温度下,向一个容积可变的容器中,通入3
mol SO2和2 mol O2及固体催化剂,使之发生反应:2SO2(g)+O2(g)  2SO3(g);ΔH=-196.6 kJ·mol-1,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4
mol SO2、3 mol O2、2 mol SO3(g),下列说法正确的是( )
2SO3(g);ΔH=-196.6 kJ·mol-1,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4
mol SO2、3 mol O2、2 mol SO3(g),下列说法正确的是( )
A.第一次平衡时反应放出的热量为294.9 kJ
B.两次平衡SO2的转化率相等
C.第二次达平衡时SO3的体积分数大于
D.达平衡时用O2表示的反应速率为0.25 mol·L-1·min-1
B
【解析】设第一次达平衡时生成SO3(g)的物质的量为2x,则剩余SO2(g)的物质的量为(3-2x)、O2(g)为(2-x),混合气体总的物质的量为(5-x),根据阿伏加德罗定律有5/(5-x)=1/0.9,解得x=0.5 mol,再结合热化学方程式可知,放出的热量为196.6 kJ/2=98.3 kJ。选项B,起始物质的量改为4 mol SO2、3 mol O2、2 mol SO3(g),相当于加入6 mol SO2、4 mol O2,n(SO2)/n(O2)=3/2,故与第一次平衡是等效平衡,两次平衡中SO2的转化率、SO3的体积分数相等,故选项B正确,C错误。选项D,条件不足,无法计算反应速率。

(2011·吉林省实验中学模考)在一定温度下,向一个容积可变的容器中,通入3 mol SO2和2 mol O2及固体催化剂,使之发生反应:2SO2(g)+O2(g) 2SO3(g);ΔH=-196.6 kJ·mol-1,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4 mol SO2、3 mol O2、2 mol SO3(g),下列说法正确的是( )
2SO3(g);ΔH=-196.6 kJ·mol-1,平衡时容器内气体压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4 mol SO2、3 mol O2、2 mol SO3(g),下列说法正确的是( )
| A.第一次平衡时反应放出的热量为294.9 kJ |
| B.两次平衡SO2的转化率相等 |
| C.第二次达平衡时SO3的体积分数大于 |
| D.达平衡时用O2表示的反应速率为0.25 mol·L-1·min-1 |
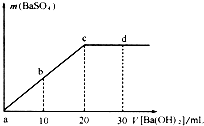 (2011?浦东新区一模)如图,常温下,向一定体积的0.1mol/L的硫酸溶液中逐滴加入浓度相同的Ba(OH)2溶液,生成沉淀的量与加入Ba(OH)2溶液的体积关系,a、b、c、d分别表示实验中不同阶段的溶液,下列有关说法中不正确的是( )
(2011?浦东新区一模)如图,常温下,向一定体积的0.1mol/L的硫酸溶液中逐滴加入浓度相同的Ba(OH)2溶液,生成沉淀的量与加入Ba(OH)2溶液的体积关系,a、b、c、d分别表示实验中不同阶段的溶液,下列有关说法中不正确的是( )