题目内容
欲使1L 0.5mol/L的NaOH溶液的浓度增大一倍,可采取的合理措施是( )
| A、加入20g固体NaOH,搅拌、溶解 |
| B、将溶液加热浓缩至0.2L |
| C、加入10mol/L的NaOH溶液0.1L,再稀释至1.5L |
| D、加入1L 1.5mol/L的NaOH溶液混合均匀 |
考点:溶液的配制
专题:化学实验基本操作
分析:A.20g氢氧化钠的物质的量为0.5mol,向1L溶液中进入0.5mol氢氧化钠固体,溶液的体积会发生变化,所以溶液浓度不等于1mol/L;
B.将溶液加热浓缩至0.2L,溶液的浓度变为原先的:
=5倍;
C.先计算出氢氧化钠的总物质的量,然后根据c=
计算出所得溶液的浓度;
D.两溶液混合后溶液的体积会发生变化,混合液体积不等于2L.
B.将溶液加热浓缩至0.2L,溶液的浓度变为原先的:
| 1L |
| 0.2L |
C.先计算出氢氧化钠的总物质的量,然后根据c=
| n |
| V |
D.两溶液混合后溶液的体积会发生变化,混合液体积不等于2L.
解答:
解:A.加入20g固体NaOH,搅拌、溶解,由于溶解后的溶液体积会发生变化,氢氧化钠的物质的量为1mol,但是溶液的体积不是1L,所以浓度不是1mol/L,故A错误;
B.将溶液加热浓缩至0.2L,溶液的浓度变为原先的:
=5倍,浓缩后溶液的浓度为:0.5mol/L×5=2.5mol/L,故B错误;
C.加入10mol/L的NaOH溶液0.1L,再稀释至1.5L,此时溶液中氢氧化钠的浓度为:c(NaOH)=
=1mol/L,浓度变为原先的2倍,故C正确;
D.加入1L 1.5mol/L的NaOH溶液混合均匀,混合液的体积不是2.5L,所得溶液的浓度也不是 1mol/L,故D错误;
故选C.
B.将溶液加热浓缩至0.2L,溶液的浓度变为原先的:
| 1L |
| 0.2L |
C.加入10mol/L的NaOH溶液0.1L,再稀释至1.5L,此时溶液中氢氧化钠的浓度为:c(NaOH)=
| 0.5mol/L×1L+10mol/L×0.1L |
| 1.5L |
D.加入1L 1.5mol/L的NaOH溶液混合均匀,混合液的体积不是2.5L,所得溶液的浓度也不是 1mol/L,故D错误;
故选C.
点评:本题考查了一定物质的量浓度的溶液配制方法,题目难度不大,注意掌握物质的量浓度的概念及配制一定浓度的溶液的方法,明确溶液混合后溶液的体积不能简单的加和.

练习册系列答案
相关题目
将a molNa2O2和b mol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应.当排出气体为两种气体时,a:b的值不可能是( )
| A、1:1 | B、1:2 |
| C、2:3 | D、3:2 |
金属钠放在水中浮在水面上,放在煤油中沉在油层下,煤油的密度是0.8g?cm-3,推测钠的密度(g?cm-3)( )
| A、大于1.0g?cm-3 |
| B、小于0.8g?cm-3 |
| C、介于0.8~1.0g?cm-3之间 |
| D、不能确定 |
CrO5的结构式为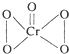 ,据此推断该氧化物( )
,据此推断该氧化物( )
 ,据此推断该氧化物( )
,据此推断该氧化物( )| A、稳定性比较高,不易分解 |
| B、稳定性比较低,易分解 |
| C、分子中所有原子均达到8电子稳定结构 |
| D、属于碱性氧化物 |
用密度为1.32g/cm3的硫酸溶液逐滴滴入到氢氧化钡溶液中,直到沉淀恰好完全为止.已知生成沉淀的质量等于原硫酸溶液的质量,硫酸溶液中溶质的质量分数是( )
| A、42.1% |
| B、43.1% |
| C、44.1% |
| D、45.1% |
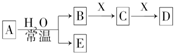 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断不正确的是( )
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断不正确的是( )| A、若A是单质,B和D的反应是OH-+HCO3-═H2O+CO32-,则E是一种清洁能源 |
| B、若D为CO,C能和E反应,则A一定为Na2O2 |
| C、若X是Na2CO3,C为含极性键的分子,则A一定是氯气,且D和E能发生反应 |
| D、若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐 |
不用其他试剂无法鉴别的一组溶液是( )
| A、氯化铁溶液和氯化铜溶液 |
| B、盐酸和碳酸氢钠溶液 |
| C、氯化铝溶液和氢氧化钠溶液 |
| D、硫酸溶液和碳酸钠溶液 |
下列说法不正确的是( )
| A、在医疗上,碳酸氢钠是治疗胃酸过多症的一种药剂 |
| B、工业上生产漂粉精,是通过氯气与石灰水作用制成的 |
| C、高性能通信材料光导纤维的主要原料是二氧化硅 |
| D、空气中的NO2是造成光化学烟雾的主要因素 |
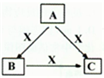 A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(其它产物已略去),下列说法错误的是( )
A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(其它产物已略去),下列说法错误的是( )| A、若X为O2,则A可为硫化氢 |
| B、若X为KOH溶液,则A可能为AlCl3 |
| C、若X为Fe,则C可能为Fe(NO3)2 |
| D、若A、B、C均为焰色反应呈黄色的化合物,则X可能为Na |