题目内容
碳酸锰(MnCO3)是理想的高性能强磁性材料,也是制备Mn2O3、MnO2等锰的氧化物的重要原料,广泛用于电子、化工、医药等行业.一种制备MnCO3的生产流程如图所示.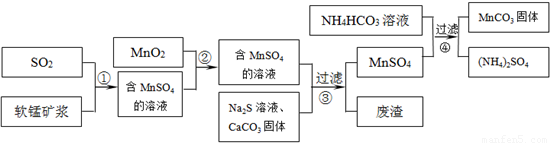
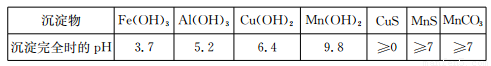
已知生成氢氧化物的pH和有关硫化物的Ksp如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 |
| 物质 | MnS | CuS | PbS |
| Ksp | 2.5×10-13 | 6.3×10-36 | 8.0×10-28 |
(1)流程①中所得MnSO4溶液的pH比软锰矿浆的pH______(填“大”或“小”),该流程可与______(填工业生产名称)联合,生产效益更高.
(2)反应②的目的是将溶液中的Fe2+氧化成Fe3+,其离子反应方程式为______,这样设计的目的和原理是______
(3)反应③中硫化钠的作用是使重金属离子转化为硫化物沉淀,碳酸钙的作用是______.
(4)反应④发生的化学反应为:MnSO4+2NH4HCO3=MnCO3↓+(NH4)2SO4+CO2↑+H2O.
反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4.加入稍过量的NH4HCO3的目的是______,溶液的pH不能过低的原因是______.
(5)软锰矿中锰的浸出有两种工艺:
工艺A:软锰矿浆与含SO2的工业废气反应 工艺B:软锰矿与煤炭粉混合,焙烧后加稀硫酸溶解.
其中工艺A的优点是______.(答对1个即可)
【答案】分析:(1)软锰矿浆是二氧化锰,MnSO4溶液水解显酸性,Fe3+将SO2氧化为硫酸;
(2)MnO2可将Fe2+氧化成Fe3+,Fe3+完全沉淀的pH较Fe2+低;
(3)碳酸钙与溶液中的H+反应,使溶液中的PH升高;
(4)加入一种反应物能提高另一种反应物的装化率;MnCO3,NH4HCO3与酸反应;
(5)锰矿与煤炭粉混合,焙烧生成二氧化硫,污染空气.
解答:解:(1)软锰矿浆是二氧化锰,MnSO4溶液水解先酸性,根据2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.Fe3+可将SO2氧化为硫酸,故答案为:小;工业制备硫酸;
(2)MnO2可将Fe2+氧化成Fe3+,Fe3+完全沉淀的pH较Fe2+低;故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;使Fe2+ 转变为Fe3+,Fe3+完全沉淀的pH较低(或Fe3+更易沉淀);
(3)碳酸钙与溶液中的H+反应,使溶液中的PH升高,使溶液中的Fe3+、Al3+转化为氢氧化物沉淀,故答案为:与溶液中的酸反应,使溶液中的Fe3+、Al3+转化为氢氧化物沉淀;
(4)加入稍过量的NH4HCO3能提高MnSO4的装化率,使MnCO3沉淀完全,溶液的pH不过低,H+可与MnCO3,NH4HCO3反应,故答案为:使MnCO3沉淀完全;MnCO3沉淀量少,NH4HCO3与酸反应.(或MnCO3、NH4HCO3与酸反应溶解);
(5)锰矿与煤炭粉混合,焙烧生成二氧化硫,污染空气,而工艺A不仅不产生二氧化硫,且能生产硫酸,故答案为:节约能源、治理含SO2的工业废气等.
点评:本题考查制备实验方案的设计,注意一些不常见方程式的书写.
(2)MnO2可将Fe2+氧化成Fe3+,Fe3+完全沉淀的pH较Fe2+低;
(3)碳酸钙与溶液中的H+反应,使溶液中的PH升高;
(4)加入一种反应物能提高另一种反应物的装化率;MnCO3,NH4HCO3与酸反应;
(5)锰矿与煤炭粉混合,焙烧生成二氧化硫,污染空气.
解答:解:(1)软锰矿浆是二氧化锰,MnSO4溶液水解先酸性,根据2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.Fe3+可将SO2氧化为硫酸,故答案为:小;工业制备硫酸;
(2)MnO2可将Fe2+氧化成Fe3+,Fe3+完全沉淀的pH较Fe2+低;故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;使Fe2+ 转变为Fe3+,Fe3+完全沉淀的pH较低(或Fe3+更易沉淀);
(3)碳酸钙与溶液中的H+反应,使溶液中的PH升高,使溶液中的Fe3+、Al3+转化为氢氧化物沉淀,故答案为:与溶液中的酸反应,使溶液中的Fe3+、Al3+转化为氢氧化物沉淀;
(4)加入稍过量的NH4HCO3能提高MnSO4的装化率,使MnCO3沉淀完全,溶液的pH不过低,H+可与MnCO3,NH4HCO3反应,故答案为:使MnCO3沉淀完全;MnCO3沉淀量少,NH4HCO3与酸反应.(或MnCO3、NH4HCO3与酸反应溶解);
(5)锰矿与煤炭粉混合,焙烧生成二氧化硫,污染空气,而工艺A不仅不产生二氧化硫,且能生产硫酸,故答案为:节约能源、治理含SO2的工业废气等.
点评:本题考查制备实验方案的设计,注意一些不常见方程式的书写.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
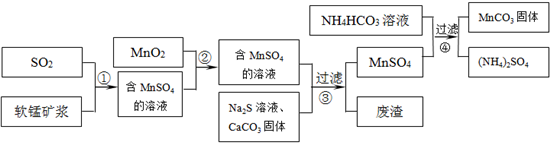
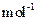 :MnCO3 115 MnO2 87 MnO 71)
:MnCO3 115 MnO2 87 MnO 71)
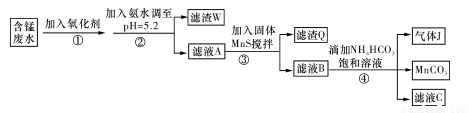
 :MnCO3 115
MnO2 87 MnO 71)
:MnCO3 115
MnO2 87 MnO 71)