题目内容
【题目】己知:CH4(g)+2H2S(g)![]() CS2(g)+4H2(g)。向恒容密闭容器中充入0.lmolCH4和0.2molH2S,如图所示:
CS2(g)+4H2(g)。向恒容密闭容器中充入0.lmolCH4和0.2molH2S,如图所示:

下列说法不正确的是
A.该反应的△H>0
B.X点CH4的转化率为20%
C.X点与Y点容器内压强比为55:51
D.维持Z点温度,向容器中再充入CH4、H2S、CS2、H2各0.1mol时v(正)<v(逆)
【答案】C
【解析】
A.由图,温度越高,生成物的物质的量越大,则升高温度平衡正向移动,正反应为吸热反应,则△H>0,故A正确;
B.X 点CH4的物质的量与氢气相等,则
CH4(g)+2H2S(g)![]() CS2(g)+4H2(g)
CS2(g)+4H2(g)
开始 0.1 0.2 0 0
转化 x 2x x 4x
平衡 0.1-x 0.2-2x x 4x
0.1-x=4x,解得x=0.02,则X 点CH4的转化率为0.02/0.1×100%=20%,故B正确;
C.同温同体积,物质的量与压强成正比,而X点与Y点的温度不同,则无法计算容器内压强比,故C错误;
D.Z点CH4的物质的量与CS2相等,则
CH4(g)+2H2S(g)![]() CS2(g)+4H2(g)
CS2(g)+4H2(g)
开始 0.1 0.2 0 0
转化 x 2x x 4x
平衡 0.1-x 0.2-2x x 4x
所以有0.1-x=x,解得x=0.05,各物质的量分别为0.05mol、0.1mol、0.05mol、0.2mol,设体积为V,则平衡常数K=0.16/V2,维持Z点温度,向容器中再充入CH4、H2S、CS2、H2 各0.1mol 时,物质的量分别为0.15mol、0.2mol、0.15mol、0.3mol,此时则Qc=0.2025/V2>K,则平衡逆向移动,v(正)<v(逆),故D正确;
故选:C。

【题目】(1)硝基苯甲酸乙酯在OH-存在下发生水解反应:O2NC6H4COOC2H5+OH-O2NC6H4COO-+C2H5OH。两种反应物的初始浓度均为0.050 mol·L-1,15℃时测得O2NC6H4COOC2H5的浓度c随时间变化的数据如下表所示。回答下列问题:
t/s | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
c/mol/L | 0.050 | 0.036 | 0.030 | 0.026 | 0.022 | 0.017 | 0.016 | 0.015 | 0.015 |
计算该反应在120~180s间的平均反应速率v(OH-)=_________;比较120~180s与180~240 s 区间的平均反应速率的大小,前者___________后者(填>,<或=),理由是:____________。
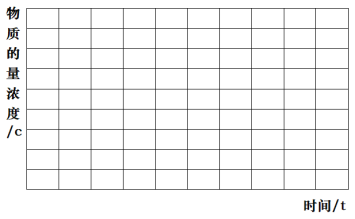
(2)某研究小组在实验室将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,温度恒定,固体试样体积忽略不计),t1时刻,反应:NH2COONH4(s)2NH3(g)+CO2(g)达到分解平衡。请在图中画出容器内NH3和CO2的物质的量浓度随时间变化的趋势图:_________
(3)工业上合成尿素的反应为:2NH3(g)+CO2(g)CO(NH2)2(s) +H2O(g) 。在一定温度和压强下,往容积可变的密闭容器内通入物质的量各为1mol的氨气和二氧化碳发生上述反应。下列说法中能说明该反应一定达到化学平衡的是_______________。
A.断裂amol的N—H键的同时消耗a/2 mol的尿素
B.密闭容器中二氧化碳的体积分数保持不变
C.密闭容器中混合气体的密度保持不变
D.密闭容器中混合气体的平均摩尔质量保持不变