题目内容
国际纯粹与应用化学联合会(IUPAC)将117号元素暂时命名为Uus,以下关于Uus的叙述正确的是
A.是稀有气体 B.有放射性 C.是第六周期元素 D.质量数为117
B
解析试题分析:117号元素是第七周期元素,都是放射性元素,B正确。
考点:本题考查元素的位与性两者的关系。

练习册系列答案
相关题目
两种短周期元素X和Y形成的单质能与氢气反应生成HX和HY,反应热分别为Q1和Q2,已知Q1>Q2,,则判断一定正确的是
| A.沸点:HY>HX | B.还原性:HY>HX |
| C.稳定性:HY>HX | D.酸性:HXO4>HYO4 |
X、Y、Z、M、N代表五种金属,有以下化学反应:
①水溶液中:X+Y2+=X2++Y;
②Z+2H2O(冷)=Z(OH)2+H2↑;
③M、N为电极与N盐溶液组成原电池,负极反应为:M-2e-=M2+;
④Y可以溶于稀H2SO4中,M不能被H2SO4氧化,则这五种金属的活动性由弱到强的顺序是
| A.M<N<Y<X<Z | B.N<M<Y<X<Z |
| C.N<M<X<Y<Z | D.X<Z<N<M<Y |
X、Y、Z三种短周期元素在周期表中的位置如图所示,Y原子的最外层电子数是次外层电子数的3倍,下列说法正确的是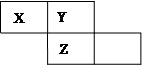
| A.气态氢化物的沸点:Z<Y |
| B.Z元素的氧化物对应的水化物一定是一种强酸 |
| C.三种元素原子半径的大小顺序为: X>Y>Z |
| D.Z单质与Fe反应生成的化合物中,铁元素显+3价 |
符号“3px”没有给出的信息是
| A.电子层 | B.电子亚层 |
| C.电子云在空间的伸展方向 | D.电子的自旋方向 |
下列说法错误的是
| A.同主族元素的简单阴离子还原性越强,水解程度越大 |
| B.Na和Cs属于IA族元素,Cs失电子的能力比Na强 |
| C.IA族与VIIA族元素间可形成共价化合物或离子化合物 |
| D.同周期元素(0族元素除外)从左到右,原子半径逐渐减小 |
X、Y为短周期元素,X位于ⅠA族,X与Y可形成化合物X2Y,下列说法正确的是
| A.X的原子半径一定大于Y的原子半径 |
| B.X与Y的简单离子不可能具有相同的电子层结构 |
| C.两元素形成的化合物中,原子个数比不可能为1∶1 |
| D.X2Y可能是离子化合物,也可能是共价化合物 |
具有下列电子层结构的原子,其相应元素一定属于同一主族的是
| A.3p轨道上有2个未成对电子的原子和4p轨道上有2个未成对电子的原子 |
| B.3p轨道上只有1个空轨道的原子和4p轨道上只有1个空轨道的原子 |
| C.最外层电子排布为1s2的原子和最外层电子排布为2s22p6的原子 |
| D.最外层电子排布为1s2的原子和最外层电子排布为2s2的原子 |
X和Y属短周期元素,X原子的最外层电子数是次外层的2倍,Y位于X的前一周期,且最外层只有一个电子,则X和Y形成的化合物的分子式可表示为( )
| A.XY | B.XY2 | C.Y3X | D.XY4 |