题目内容
CH4在一定条件下催化氧化可以生成C2H4和C2H6(水和其他反应产物忽略不计)。取一定量CH4经催化氧化后得到一种混合气体,它在标准状况下的密度为
φ(C2H4)=4.44%
解析:该题是信息给予题。CH4经催化氧化可以生成C2H4和C2H6是本题的计算依据,由混合气体(剩余CH4、C2H4和C2H6)的密度可列出等式进行计算。本题有多种解法,下面只介绍两种常见解法。
方法Ⅰ:(从消耗甲烷的物质的量入手):
设反应前CH4为1 mol,其中有x mol转化成乙烯(2CH![]() C
C![]() mol C2H4,生成C2H6
mol C2H4,生成C2H6![]() mol,则反应后混合气体的总物质的量为:(剩余CH4、生成乙烯、乙烷)。
mol,则反应后混合气体的总物质的量为:(剩余CH4、生成乙烯、乙烷)。
![]()
根据密度定义得(CH4相对分子质量为16,C2H4相对分子质量为28,C2H6相对分子质量为30)

解得x=0.080 0 mol
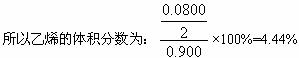
方法Ⅱ:(从生成C2H4的体积分数入手)
设反应前CH4为1 mol,消耗了20%,则反应后混合气体的总物质的量为:
![]()
又设混合气体中乙烯的体积分数为x,则
![]()
解得x=4.44%

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目