题目内容
(2013?和平区二模)下列图示与对应的叙述相符的是( )
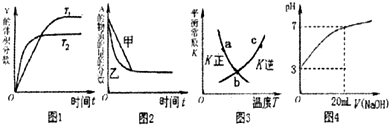

分析:A.由图可知,温度T2先到达平衡,故温度T1<T2,可逆反应2X(g)?Y(g)△H<0,正反应为放热反应,升高温度平衡向逆反应移动,Y的含量降低;
B.增大压强反应速率加快,平衡向正反应移动,平衡时A的物质的量降低;
C.图象为正、逆平衡常数与温度关系,曲线上各点都是平衡点;
D.20mL pH=3的醋酸溶液中滴加20mLpH=11的NaOH溶液,由于HAc是弱电解质,反应后为HAc、NaAc混合溶液,HAc浓度远大于NaAc,溶液呈酸性.
B.增大压强反应速率加快,平衡向正反应移动,平衡时A的物质的量降低;
C.图象为正、逆平衡常数与温度关系,曲线上各点都是平衡点;
D.20mL pH=3的醋酸溶液中滴加20mLpH=11的NaOH溶液,由于HAc是弱电解质,反应后为HAc、NaAc混合溶液,HAc浓度远大于NaAc,溶液呈酸性.
解答:解:A.由图可知,温度T2先到达平衡,故温度T1<T2,可逆反应2X(g)?Y(g)△H<0,正反应为放热反应,升高温度平衡向逆反应移动,Y的含量降低,图象与实际相符合,故A正确;
B.增大压强反应速率加快,平衡向正反应移动,平衡时A的物质的量降低,图象中到达平衡时间相同,且平衡时A的物质的量相同,图象与实际不符合,故B错误;
C.图象为正、逆平衡常数与温度关系,曲线上各点都是平衡点,故C错误;
D.20mL pH=3的醋酸溶液中滴加20mLpH=11的NaOH溶液,由于HAc是弱电解质,反应后为HAc、NaAc混合溶液,HAc浓度远大于NaAc,溶液呈酸性,图象中为中性,图象与实际不符,故D错误;
故选A.
B.增大压强反应速率加快,平衡向正反应移动,平衡时A的物质的量降低,图象中到达平衡时间相同,且平衡时A的物质的量相同,图象与实际不符合,故B错误;
C.图象为正、逆平衡常数与温度关系,曲线上各点都是平衡点,故C错误;
D.20mL pH=3的醋酸溶液中滴加20mLpH=11的NaOH溶液,由于HAc是弱电解质,反应后为HAc、NaAc混合溶液,HAc浓度远大于NaAc,溶液呈酸性,图象中为中性,图象与实际不符,故D错误;
故选A.
点评:本题以图象形式,考查化学平衡影响因素、平衡常数、溶液PH值判断等,做题时要注意从图象中获取正确信息,综合性较强,难度中等.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
