题目内容
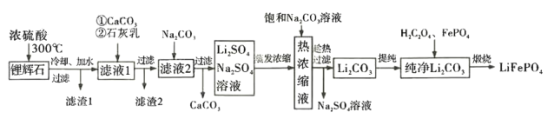
【题目】2019 年诺贝尔化学奖用于奖励对锂离子电池的发展做出贡献的三位科学家。锂离子电池如今被用于各个领域,使一个无化石燃料的社会成为可能。LiFePO4是新型锂离子电池的正极材料。某小组拟设计以一种锂辉石(主要成分为Li2O Al2O34SiO2,含少量铁、钙、镁)为原料制备纯净的碳酸锂,进而制备LiFePO4的工艺流程:
已知:Li2OAl2O34SiO2+H2SO4(浓)![]() Li2SO4+Al2O34SiO2H2O↓回答下列问题:
Li2SO4+Al2O34SiO2H2O↓回答下列问题:
(1)LiFePO4 中铁元素的化合价为_____,铁元素进行焰色反应的颜色是_______(填序号)。
A.无焰色反应 B.黄色 C.紫色 D.砖红色
(2)向滤液 1 中加入适量的 CaCO3 细粉用于消耗硫酸并将 Fe3+转化为红褐色沉淀,若![]() =3,反应的化学方程式为___;滤渣2 的主要成分是 Fe(OH)3、___(填化学式)
=3,反应的化学方程式为___;滤渣2 的主要成分是 Fe(OH)3、___(填化学式)
(3)已知碳酸锂在水中的溶解度随温度升高而减小,上述流程中趁热过滤的目的是__。
(4)流程中加H2C2O4和FePO4,用于煅烧制备 LiFePO4,该反应的化学方程式为____。
(5)若滤液1中c(Mg2+)=0.2 mol/L,向其中加入双氧水和磷酸(设溶液体积增加 1 倍),使Fe3+恰好沉淀完全即溶液中 c(Fe3+)=1.0×10-5 mol/L,此时是否有 Mg3 (PO4)2 沉淀生成?_____(列式计算说明)。已知 FePO4 、Mg3 (PO4)2 的 Ksp 分别为 1.3×10-22、1.0×10-24。(6)一种锂离子电池的反应原理为 LiFePO4![]() Li+FePO4。写出放电时正极电极反应式: ____。
Li+FePO4。写出放电时正极电极反应式: ____。
【答案】+2 A Fe2(SO4)3+3H2SO4+6CaCO3= 2Fe(OH)3+6CaSO4+6CO2↑ Mg(OH)2 CaSO4 减小 Li2CO3 的溶解损失 Li2CO3+H2C2O4+2FePO4 ![]() 2LiFePO4+3CO2↑+H2O↑ 由 Ksp(FePO4)可知 c(PO
2LiFePO4+3CO2↑+H2O↑ 由 Ksp(FePO4)可知 c(PO![]() )=
)= ![]() =1.3×10-17mol·L-1;Qc[Mg3(PO4)2]= c3(Mg2+)· c2(PO
=1.3×10-17mol·L-1;Qc[Mg3(PO4)2]= c3(Mg2+)· c2(PO![]() )=
)=![]() ×(1.3×10-17mol·L-1)2=1.69×10-37<Ksp,因此不会生成 Mg3(PO4)2 沉淀 FePO4+ Li ++e-=LiFePO4
×(1.3×10-17mol·L-1)2=1.69×10-37<Ksp,因此不会生成 Mg3(PO4)2 沉淀 FePO4+ Li ++e-=LiFePO4
【解析】
锂辉石(主要成分为Li2O·Al2O3·4SiO2,含少量铁、钙、镁)加入浓硫酸共热,根据已知信息可知得到的滤渣1主要成分为Al2O3·4SiO2·H2O,滤液中的主要阳离子有Fe3+、Mg2+、Ca2+、Li+;加入碳酸钙和石灰乳可以将过量的氢离子和Fe3+、Mg2+除去,滤渣2主要为Fe(OH)3、Mg(OH)2以及硫酸钙;滤液主要杂质离子有Ca2+和SO42-;再加入碳酸钠将钙离子除去,得到硫酸锂和硫酸钠的混合溶液,蒸发浓缩后加入饱和碳酸钠溶液,趁热过滤得到碳酸锂沉淀;提纯后加入草酸和磷酸铁经煅烧得到LiFePO4。
(1)由化合价代数和等于0得:LiFePO4 中铁元素的化合价为+2价,铁元素进行焰色反应的颜色是无焰色反应,故答案为:+2;A;
(2)向滤液 1 中加入适量的 CaCO3 细粉用于消耗硫酸并将 Fe3+转化为红褐色沉淀,若![]() =3,溶液中有过量的硫酸,所以方程式为Fe2(SO4)3+3H2SO4+6CaCO3= 2Fe(OH)3+6CaSO4+6CO2↑;根据分析可知滤渣2的主要成分是Fe(OH)3、Mg(OH)2以及CaSO4;故答案为:Fe2(SO4)3+3H2SO4+6CaCO3= 2Fe(OH)3+6CaSO4+6CO2↑;Mg(OH)2以及CaSO4;
=3,溶液中有过量的硫酸,所以方程式为Fe2(SO4)3+3H2SO4+6CaCO3= 2Fe(OH)3+6CaSO4+6CO2↑;根据分析可知滤渣2的主要成分是Fe(OH)3、Mg(OH)2以及CaSO4;故答案为:Fe2(SO4)3+3H2SO4+6CaCO3= 2Fe(OH)3+6CaSO4+6CO2↑;Mg(OH)2以及CaSO4;
(3)已知碳酸锂在水中的溶解度随温度升高而减小,上述流程中趁热过滤的目的是减小碳酸锂的溶解度,减少碳酸锂的溶解损耗;故答案为:减少碳酸锂的溶解损耗;
(4)流程中加H2C2O4和FePO4,煅烧制备过程的原料为Li2CO3、H2C2O4和FePO4,产物中有LiFePO4,铁元素的化合价降低,则该过程中某种物质被氧化,根据元素化合价变化规律可知草酸中的C元素被氧化,由+3价升高为+4价,结合电子守恒和元素守恒可知方程式为:Li2CO3+H2C2O4+2FePO4![]() 2LiFePO4+3CO2↑+H2O↑。故答案为:Li2CO3+H2C2O4+2FePO4
2LiFePO4+3CO2↑+H2O↑。故答案为:Li2CO3+H2C2O4+2FePO4 ![]() 2LiFePO4+3CO2↑+H2O↑;
2LiFePO4+3CO2↑+H2O↑;
(5)若滤液1中c(Mg2+)=0.2 mol·L-1,向其中加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中 c(Fe3+)=1.0×10-5mol·L-1,由 Ksp(FePO4)可知 c(PO![]() )=
)= ![]() =1.3×10-17mol·L-1;Qc[Mg3(PO4)2]= c3(Mg2+)· c2(PO
=1.3×10-17mol·L-1;Qc[Mg3(PO4)2]= c3(Mg2+)· c2(PO![]() )=
)=![]() ×(1.3×10-17mol·L-1)2=1.69×10-37<Ksp,因此不会生成 Mg3(PO4)2 沉淀。故答案为:由 Ksp(FePO4)可知 c(PO
×(1.3×10-17mol·L-1)2=1.69×10-37<Ksp,因此不会生成 Mg3(PO4)2 沉淀。故答案为:由 Ksp(FePO4)可知 c(PO![]() )=
)= ![]() =1.3×10-17mol·L-1;Qc[Mg3(PO4)2]= c3(Mg2+)· c2(PO
=1.3×10-17mol·L-1;Qc[Mg3(PO4)2]= c3(Mg2+)· c2(PO![]() )=
)=![]() ×(1.3×10-17mol·L-1)2=1.69×10-37<Ksp,因此不会生成 Mg3(PO4)2 沉淀;
×(1.3×10-17mol·L-1)2=1.69×10-37<Ksp,因此不会生成 Mg3(PO4)2 沉淀;
(6)一种锂离子电池的反应原理为LiFePO4![]() Li+FePO4,放电时正极铁元素得电子,发生还原反应,电极反应式: FePO4+ Li ++e-=LiFePO4。故答案为:FePO4+Li ++e-=LiFePO4。
Li+FePO4,放电时正极铁元素得电子,发生还原反应,电极反应式: FePO4+ Li ++e-=LiFePO4。故答案为:FePO4+Li ++e-=LiFePO4。